查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





基本资料
患者:女,56岁
初诊时间:2017.8(8年前)
主诉:黏液血便10天。
既往史:无特殊,无类似肿瘤家族史。
入院查体
体格检查:BMI:22.1kg/m²,ECOG:0分,NRS-2002 1分。锁骨上、腹股沟区等浅表淋巴结无肿大;腹软,无压痛及反跳痛,未触及肿块,肛门指诊:阴性。
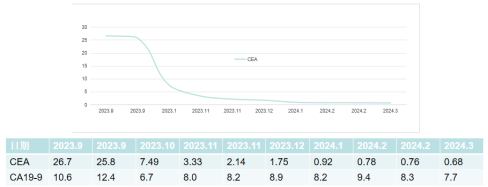
抽血检查:CEA 4ng/ml,CA19-9 10.74 U/ml。
肠镜:乙状结肠环形结节状不规则肿物,管腔狭窄,肠镜不可通过。
肠镜病理:腺癌。
胸部CT: 未见异常,建议随访。
检查资料
腹部增强MRI:乙状结肠及降结肠交界处癌,浸润浆膜层,灶周散在小淋巴结;肝Ⅴ-Ⅵ段交界处占位:考虑转移瘤(大小3.0*2.5cm)。
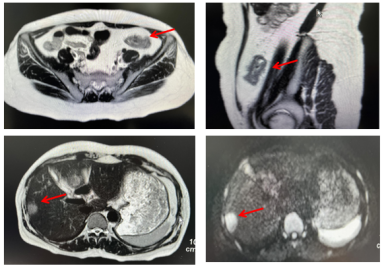
第一次MDT
首诊诊断:乙状结肠恶性肿瘤(伴同时性肝转移 c-T3N+M1a Ⅳa期)
CRS评分:2分,转移瘤数目>1个,CEA水平>200ng/ml,转移瘤最大直径>5cm,原发肿瘤淋巴结阳性,同时性肝转移。
病理科:中分化腺癌诊断明确,错配修复蛋白无缺失pMMR状态。
影像科:病灶位于乙状结肠,淋巴结阳性,肝脏占位考虑转移瘤。
肿瘤内科:CRS评分2分,治疗目标无疾病状态(NED),可考虑直接手术,术后需要联合全身治疗。
结直肠外科:原发灶可切除,手术难度不大。
肝胆外科:肝脏转移瘤可手术切除,难度不大,考虑腹腔镜手术,同期/分期切除均可。
介入科:肝转移瘤较小,3cm,介入也可以达到根治效果,如肝胆外科能手术难度不大可优先考虑肝转移切除。
拟定治疗计划:原发灶切除-间歇期化疗-肝转移切除-术后辅助化疗。
第一次原发灶手术及诊断
2017-08-09在全麻下行腹腔镜辅助下乙状结肠癌根治术。
术后病理示:乙状结肠腺癌Ⅱ级,溃疡型肿物,大小4cm×3.5cm×0.7cm,浸润至浆膜下层,见神经侵犯及脉管癌栓;区域淋巴结见癌转移(253淋巴结0/0,肠旁0/2,肿物旁18/22);上、下切缘及环周切缘未见癌。特殊染色结果:弹力纤维(+)。免疫组化结果:错配修复蛋白未见缺失,Villin(+),CK20(+),CDX-2(+),Ki67(约80%+)。
术后诊断:乙状结肠恶性肿瘤(腺癌伴肝转移 p-T3N2bM1a Ⅳa期 pMMR)
个人原因拒绝进一步查基因检测。
第二次手术及诊断
术后Capeox化疗2周期后,为防止肝转移瘤影像学消失,立即行肝转移瘤手术。于2017-10-23行腹腔镜右肝转移瘤切除术。
术后病理示:(肝脏肿物)转移性腺癌,结合病史、组织形态及免疫组化结果,符合乙状结肠来源。
术后继续Capeox化疗6周期辅助化疗(末次2018-03-07)。
遗留外周神经毒性G2,手足综合征、骨髓抑制等不良反应可耐受。第一次获得NED后随访,进入随访,每3个月复诊一次。
2019-03-18复查出现肺转移(术后17个月):(1)胸部增强CT:右肺上叶尖段占位:考虑恶性肿瘤,转移瘤?原发?(大小2.5*2.5cm)。(2)全腹部增强MRI示:乙状结肠癌根治术改变,吻合口区未见明显恶性征象;左侧前庭大腺囊肿增大,建议随访;盆底腹膜略增厚同前,盆腔微量积液;DWI上骨盆骨质弥漫信号增高同前。(3)全身骨显像:L4-5椎体血运丰富、代谢旺盛,多考虑良性病变;下颌骨左侧齿槽炎;颅骨骨质疏松改变。(4)CEA、CA19-9正常范围。
图2 术后17个月复查的影像学结果
第二次MDT
讨论结论:右肺部单发占位,原发肺癌或转移瘤未完全确定,考虑活检有一定创伤且胸腔镜手术切除难度不大,建议先行肺部病灶切除明确性质。
第三次手术及诊断
2019-04-10在全麻下行单孔胸腔镜下肺部分切除术。
术后病理:(右肺上叶)腺癌,结合免疫组化结果及病史,符合转移性结肠腺癌,肿物大小2.6cm× 2cm× 1.6cm;淋巴结未见癌转移(7组0/2,11组0/4,10组0/2)。免疫组化结果:CK7(-),CEA(+),TTF-1(+),Napsin-A(-),CK20(+),CDX-2(+),Villin(+),MUC2(-)。
诊断:1、乙状结肠恶性肿瘤(腺癌伴肝转移、肺转移 rP-T3N2bM1b Ⅳb期 pMMR),2、右上肺继发恶性肿瘤(转移性结肠腺癌) 。
完善基因检测示:MSS;Kras、Nras、BRAF、POLE/POLD1均野生型。
为减少“奥沙利铂”外周神经毒性(OIPN),ESMO 2020推荐累积剂量> 600 mg/m²时需警惕持续性神经毒性。
遗留OIPN反应 G2级:停奥沙利铂,维生素B族+度洛西汀干预。
术后于2019-07-07、2019-07-25、2019-08-10 FOLFIRI方案化疗3周期。
因无法耐受胃肠道反应,慢性腹泻。改口服“卡培他滨方案1250mg/m2 bid”单药巩固 4周期(末次2019-12-12,持续半年)。
第二次获得NED后继续随访。
2023-08-25复查发现结直肠癌腹膜后淋巴结转移(术后6年):(1)CEA:26.70ng/mL。(2)2023-08-24胸部CT:肺转移瘤术后改变,右肺上叶术区斑片索条影同前;左肺、右肺中叶及下叶新增数个粟粒、微结节,建议密切随诊;(3)2023-08-25腹部MRI:乙状结肠癌根治术改变,吻合口区未见明显恶性征象;下腹部腹膜后至双侧髂血管起始段旁新增转移淋巴结,较大者36mm×22mm;右肝转移瘤切除+部分大网膜切除术后改变。(4)PET-CT未查。
图3 2023-08-25腹部MRI
第三次MDT
评估:肺多发结节较小可密切随访,腹膜后淋巴结潜在可切除。
治疗耙器官:腹膜后转移淋巴结。
治疗目标:NED。
治疗策略:转化治疗-腹膜后转移灶清扫。
化疗方案:mFolfox6+西妥昔单抗。
每2-3个月后再评估,争取手术机会。
讨论结论:多学科MDT精准治疗促成三次NED。
转化治疗
2023-09-21~2024-03-18予“mFolfox6+西妥昔单抗”方案化疗12周期。
期间每2个月/4个周期评估一次。过程中Ⅱ度骨髓抑制,升白细胞、升血小板治疗后恢复。
化疗12周期后胸部评价:2024-04-01胸部CT:右肺下叶背段(Se4 In108)钙化结节同前。左肺上叶前段、下叶外基底段、右肺(In75 167 183)见数个微小结节同前,建议随访。
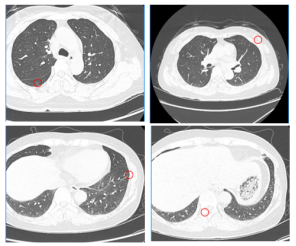
图5 化疗12周期后胸部评价
化疗12周期后腹膜后评价:2024-04-01腹膜后淋巴结情况:下腹部腹膜后至双侧髂血管起始段旁淋巴结较前明显缩小,较大者约16mm×9mm(初始约36mm×22m),未见新增病灶。
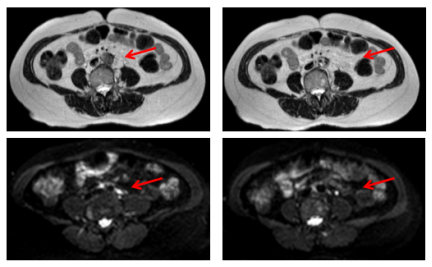
第四次MDT讨论
影像:肺微小结节建议随访,腹膜后淋巴结位于肾静脉以下,未见其他新增病灶。
内科:围手术期化疗周期足,评价部分缓解(PR)。
放疗:腹膜后也可行SBRT局部治疗(优势在于可以局部控制较好,但缺乏病理确证;依据 NCCN 2024 5.3,本例可考虑优先手术以达R0)。
外科:有腹膜后手术探查的机会。指征:清扫肾静脉水平以下的孤立性转移 PLNM(16b组,明确上、下、左、右界限,参考CSCO 2024,确保R0切除),可能为患者带来远期生存获益,R0切除后的中位生存期为34~64个月,5年总生存率(OS)为29.1%~53.4%。
综合意见:腹膜后手术探查。
第四次手术腹膜后清扫
于2024-04-22 在全麻下行腹腔镜下腹膜后淋巴结清扫术(16b组)。
术中所见:肠系膜下动静脉术后缺如,肝脏、胃、小肠、大网膜、盆底未见明显转移结节;腹主动脉分叉处到近端5cm腹膜后增厚,可触及结节样隆起,直径约1.2cm。
术后病理:(腹膜后肿物)镜下见纤维胶原增生结节,中央坏死伴钙化,周围泡沫样细胞、类上皮细胞及淋巴细胞浸润,未见癌。请结合临床。免疫组化结果:1号片:CK-P(-);2号片:CK-P(-);3号片:CK-P(-)。
考虑肿瘤病理完全缓解(pCR)。
第三次获得NED,患者仍坚持在工作岗位,生活质量良好,随访至今(末次随访2025.10.30)。
病史回顾
图7 病史回顾
个人体会
从初诊肝转移,到肺转移,再到腹膜后复发;三次面临绝境,三次在MDT的协作下获得“重生”。
每一次讨论,都是在生与死之间的抉择;每一次决策,都是团队智慧的凝结,精准把握手术窗口期。
手术的刀锋有限,而MDT的力量无限。MDT的意义,不止于延长生命,更在于给予患者一次又一次重新生活的机会。
本文审校:
福建医科大学附属漳州市医院 汪冠聪教授
查看更多