查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:首都医科大学附属北京天坛医院神经病学中心 徐芸
本期研究生园地由首都医科大学附属北京天坛医院神经病学在读博士徐芸与大家分享于2020年6月22日发表于JAMA Neurology上的“Association Between Immunosuppressive Treatment and Outcomes of Cerebral Amyloid Angiopathy–Related Inflammation”一文。
研究背景
脑淀粉样血管病相关炎症(Cerebral amyloid angiopathy-related inflammation, CAA-ri)是一种独特的脑淀粉样血管病亚型,其特征是对脑血管β-淀粉样沉积物的自身免疫反应。
临床表现不同于常见非炎症型脑淀粉样血管病,主要表现为亚急性认知改变、癫痫和血管源性水肿。CAA-ri存在自身免疫性炎症反应的证据,临床经常使用各种免疫抑制剂治疗。有观察性研究表明治疗后临床和影像学均有所改善,但目前尚不清楚CAA-ri的特殊标记物,如血管壁炎症的病理证据、脑脊液细胞增多、神经影像显示近期梗死或强化病灶等是否与更严重的病程相关。
本研究旨在明确临床、神经影像学、实验室、病理或治疗与CAA-ri发作后结局的相关性。
研究方法
本研究为一项回顾性队列研究,纳入1998年7月3日至2017年11月27日期间的连续患者数据,包括48名符合诊断标准的CAA-ri患者,他们至少有1次疾病发作和后续的结局数据,收集人口统计学、遗传学、病理学、临床、实验室、影像学、治疗和结局相关数据等。临床炎症发作定义为新的或不典型的或加重的头痛、急性或亚急性认知功能下降、癫痫发作或局灶性缺陷。
影像炎症急性发作定义为:
(1)皮质下T2WMH,通常不对称,提示脑水肿,而不是典型的脑室周围或皮质下白质病变;
(2)T1增强;或
(3)MRI局限性弥散病变。临床改善和恶化定义为神经体征或症状的持续变化。主要终点为经免疫治疗后临床症状的改善情况(分为改善、稳定、恶化)。次要终点为经免疫治疗后影像学的改善情况,以及治疗后疾病的复发率。
研究结果
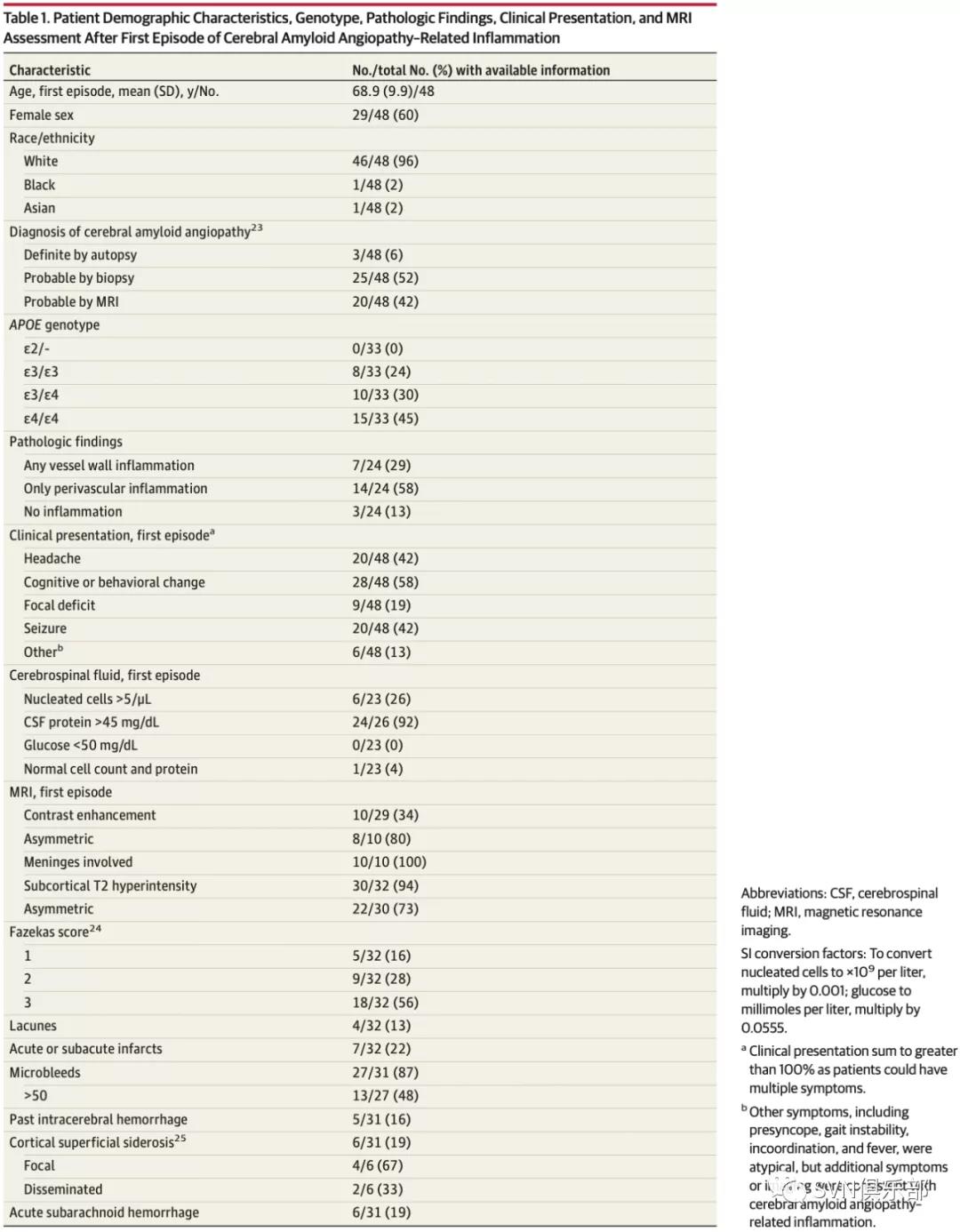
48例患者最终纳入研究,中位随访时间为2.7年(IQR 1.0~5.5年)。Table 1总结了患者的人口学及临床特征。
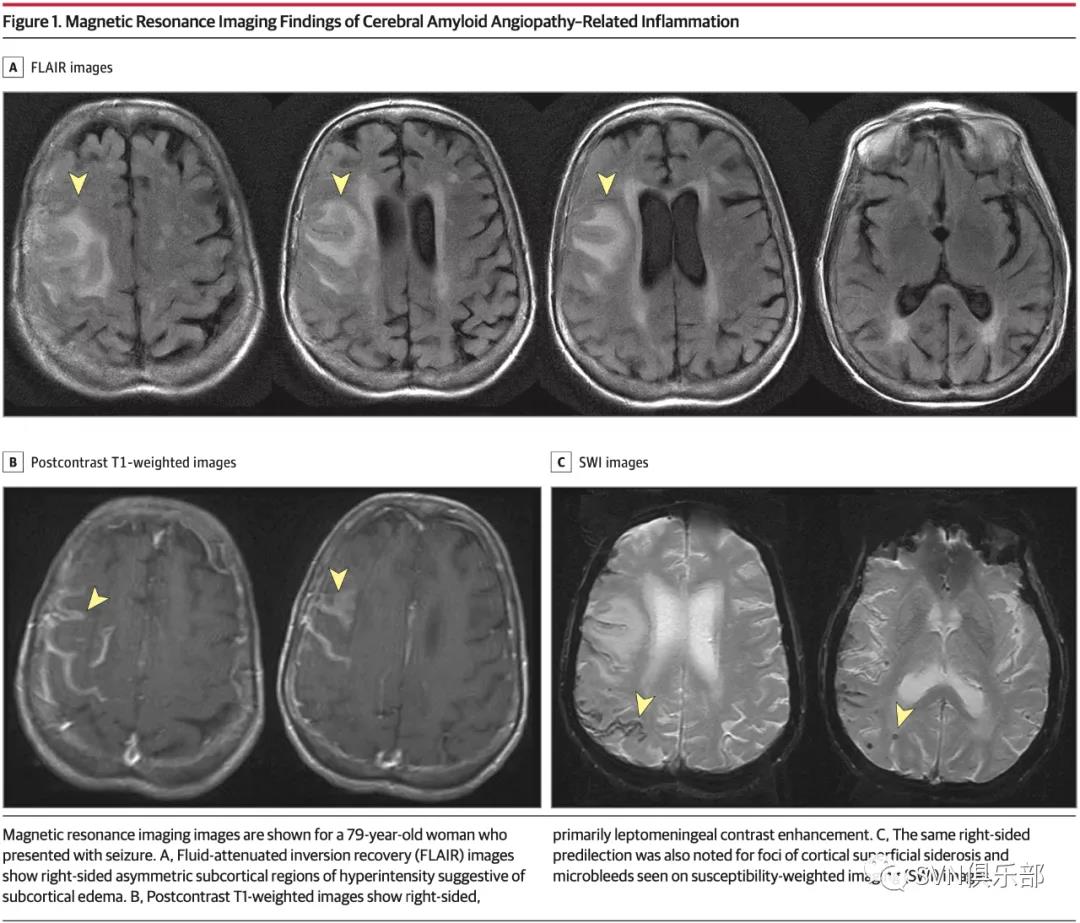
CAA-ri患者典型的MRI病灶如Figure 1所示。FLAIR示右侧不对称皮质下高信号区,T1增强显示右侧软脑膜增强,SWI显示主要分布于右侧的皮质浅表铁质沉积和微出血。
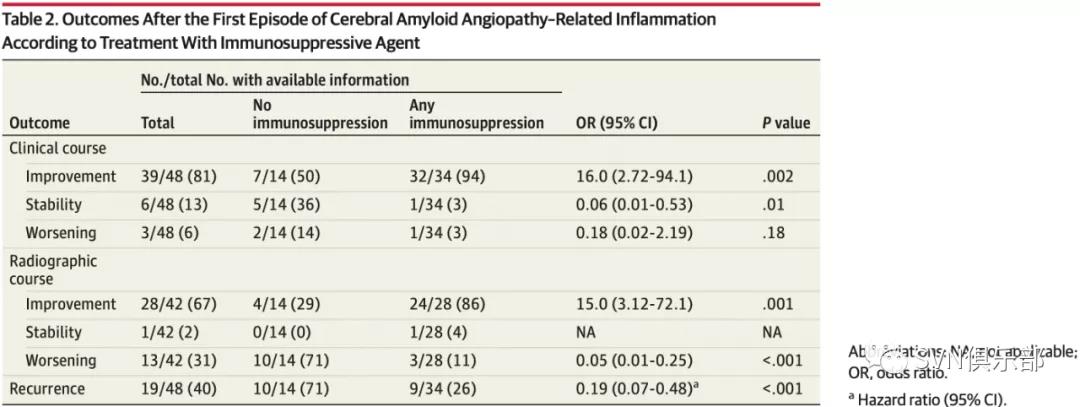
39例(81%)患者治疗后临床症状好转,6例(13%)保持稳定,3例(6%)恶化。使用任何免疫抑制剂治疗相较于不使用更有可能取得临床改善[32 of 34[94%] vs 7 of 14(50%); OR, 16.0; 95%CI, 2.72~94.1]。28例(67%)患者治疗后影像学改善,1例(2%)稳定,3例(31%)影像学恶化。治疗后影像学改善的可能性也更大[24 of 28[86%] vs 4 of 14(29%)]; OR, 15.0; 95%CI, 3.12~72.1](Table 2)。
在logistic回归分析中(Table 3),APOE ε4等位基因数量与临床改善没有显著相关性(OR, 2.68; 95%CI, 0.89~8.08)。除免疫治疗外,未发现其他与临床改善相关的因素。在单因素logistic回归分析中发现,除免疫治疗外,APOE ε4等位基因数量也与影像改善相关(OR, 6.19; 95%CI, 1.62~23.6),在控制免疫抑制治疗的多变量模型中仍然显著(OR, 4.49; 95%CI, 1.11~18.2)。
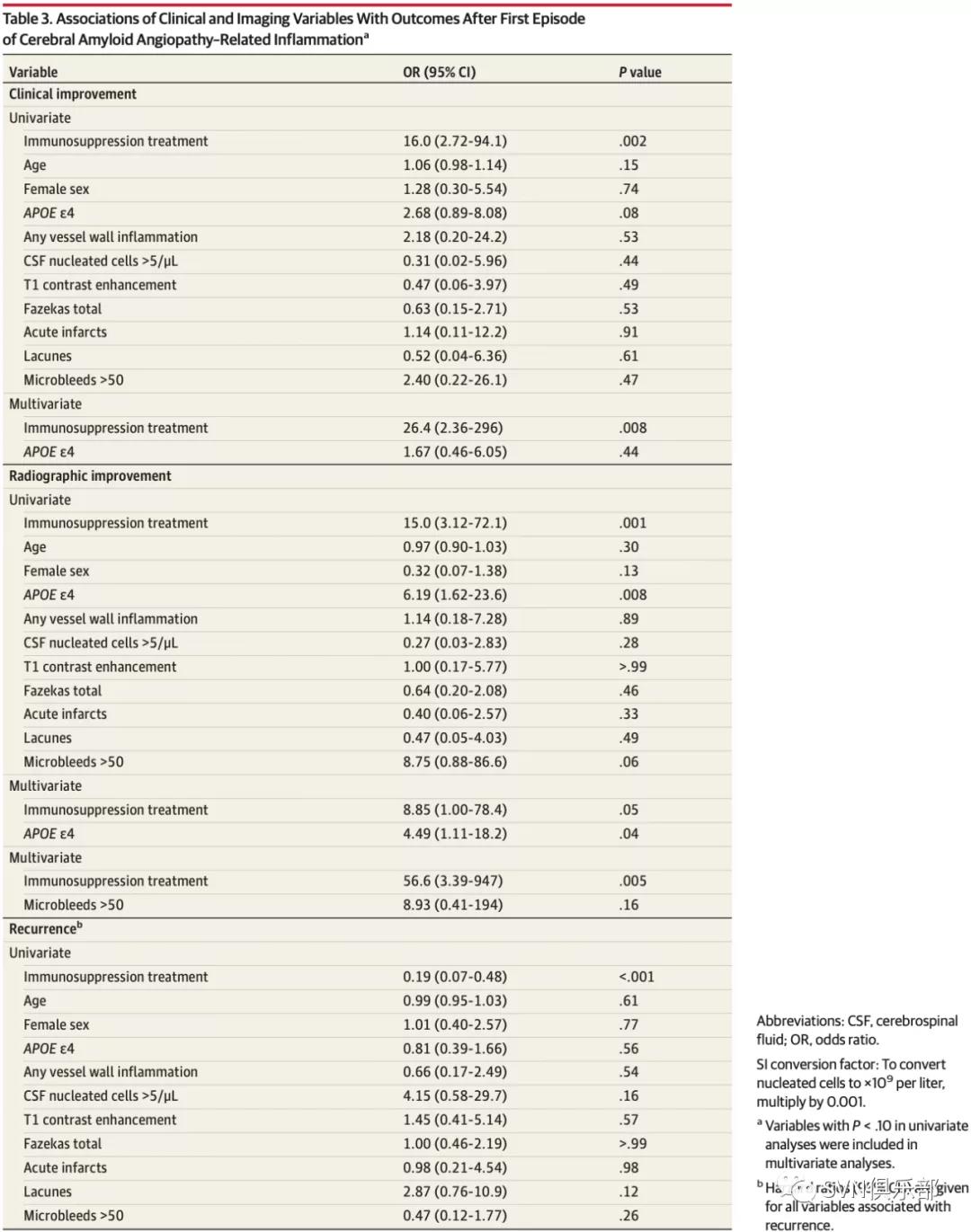
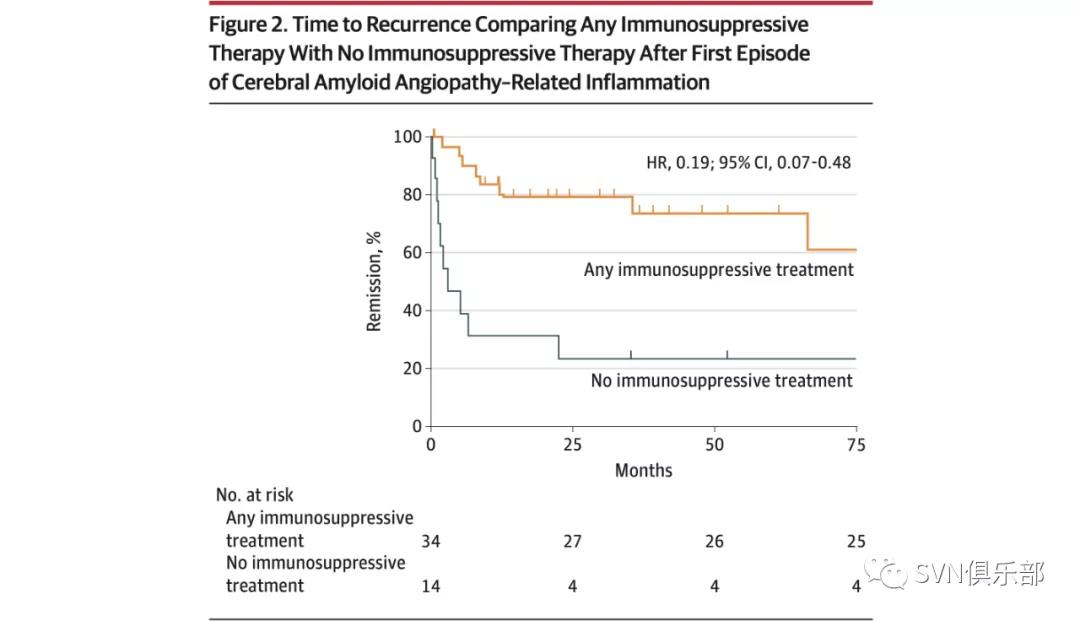
使用任何免疫抑制剂治疗相较于不使用免疫抑制剂,复发的可能性低[9/34(26%)vs. 10/14(71%); HR, 0.19; 95%CI, 0.07~0.48](Figure 2)。
Q
本研究的优点及不足主要有哪些?
A
本研究的主要优点是对这种较罕见CAA亚型进行了相对较大样本量的收集,同时进行了详细的临床、实验室、病理学和影像学分析。该研究回顾了20年间CAA-ri患者的相关数据,对该亚型患者免疫治疗的有效性及与临床预后相关的因素进行了较为全面的分析,为进一步进行临床药物试验奠定了坚实基础。但由于CAA-ri很罕见,该研究样本量较少(最终纳入48例患者),同时尚有较多的患者存在影像学相关数据的缺失,这种缺失可能会造成影像学改善这一次要结局的判断出现偏倚。但即使存在一些不足,本研究对于CAA-ri免疫治疗的探索仍有重要意义。
Q
国际公认的评价新药疗效和安全性的金标准是随机双盲对照临床试验。FDA通常需要两项随机双盲对照临床试验来支持药物批准。对于罕见病和常见病的药物临床试验设计,有什么不同呢?
A
罕见病有以下特点:(1)患病率低;(2)疾病人群异质性高;(3)疾病认识不充分,诊断困难;(4)大多数疾病严重或危及生命,医疗需求巨大;(5)缺乏公认的终点和评价方法。
目前从统计学角度来看,罕见病药物临床试验设计可以采取自身对照的病例系列研究(Self Controlled Case Series, SCCS)(SCCS设计可测量一个短暂暴露对结局的影响,它是以自身为对照,收集研究对象未暴露情况下的事件发生率,再去收集研究对象暴露情况下的事件发生率,从而计算暴露对于事件的相对影响。它的优势是不需要另外寻找对照,同时自身匹配又解决了很多混杂因素的影响)、单病例随机对照设计(单病例随机对照设计通过随机方法安排治疗期和对照期顺序,进行三轮或三轮以上的治疗周期,应用于单个病例的自身对照双盲治疗研究。
每一轮治疗之间可有一段时间的空白期,也称为“洗脱期”,以消除前一次干预措施残余的影响,使患者和实施治疗的医生对治疗顺序处于未知状态的双盲法是试验必不可少的重要条件。鉴于大样本随机对照试验的最终结果可能不适用于单个或特殊患者,单病例试验的优点在于,短时间内从多种治疗中选出最有效者,患者从试验中可直接获益,易被患者接受,失访率低)、随机撤药试验设计(randomised with drawal study, RWS)(该设计是所有患者在采用试验药物或试验疗法治疗一段时间后,再随机分为试验组和对照组。
试验组继续使用试验药物或其他干预疗法,而对照组多采用安慰剂,重点观察两组在撤药后原有的症状是否复发或加重。由于存在撤药过程,所以该试验设计非常能够体现疗效的产生是否和试验的干预手段有关)、单独目标设计、分阶段设计等方法进行。需要注意的是由于病例数很少,在开始试验设计时需要更加注重实验的科学性,设计需更加严谨。
Q
CAA-ri免疫治疗是有效的,但患者通常年龄较大。老年患者接受免疫治疗风险会更高吗?
A
免疫抑制剂相关副作用包括免疫相关皮肤毒性、内分泌疾病、肝脏毒性、胃肠毒性、肺炎等。许多关于老年癌症患者使用免疫抑制剂的研究表明,老年患者使用免疫抑制剂的风险似乎与年轻患者相似。但通常需要更严密的监测。
首先,在使用免疫抑制药物前应充分了解该药物潜在的毒性谱。其次,要做好免疫治疗前的基线检查,包括影像学的检查,脏器功能的检查等,检查的结果用于评估患者发生毒性的易感性,以及治疗期间出现不良反应时对比确认。再者,需定期进行患者用药情况评估,对免疫相关副作用进行分级管理。
Q
该研究影像学结局定义为“decreased or disappearance/increased or new of subcortical T2 WMH decreased or disappearance/increased or new of T1 enhancement”,是定性标准,而对于一项研究而言定量评估十分重要,目前可应用影像对CAA-ri进行定量评价吗?
A
CAA-ri炎症发作急性期影像学典型特征主要包括:(1)皮层下T2白质高信号,常为非对称病灶,提示脑水肿;(2)T1增强扫描可见强化病灶,脑膜强化常见;(3)DWI局限性弥散受限病变;(4)微出血。目前仅微出血病灶可通过出血点数量变化对其进行定量评估,即使应用同一型号甚至同一台仪器进行MRI扫描,其他影像学特征也可能由于体位等多种因素的变化而出现不同,导致定量评估存在较大困难。

来源:SVN俱乐部
转载已获授权,其他账号转载请联系原账号
查看更多