查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近日,复旦大学卢洪洲教授团队一项针对预防和治疗新冠病毒感染的有效药物中和抗体“MW33”注射液的临床试验表明,其安全性、耐受性、药代动力学特征等具有稳定的抗体结构和更低的免疫原性,与新冠病毒S蛋白结合后,可有效阻断病毒侵入宿主细胞,实现对病毒的中和作用。目前相关研究结果已在线发表于国际学术期刊《新发微生物与感染》(《Emerging Microbes & Infections 》)杂志8月刊。

doi: 10.1080/22221751.2021.1960900
卢洪洲教授说,除疫苗外,新冠病毒中和抗体是被普遍认可的预防和治疗新冠病毒感染的有效药物之一。而MW33注射液作为全人源B细胞单克隆中和抗体,可实现对病毒的中和作用。要使药物起到预期的作用,除要降低不良反应外,还需要明确药物的药代动力学参数,包括药物最高浓度、药物总吸收量、药物半衰期等,且参数需要表现出一定的规律,这样才能方便医生根据其药代动力学参数,通过制定合适的给药剂量和给药时间(药物浓度过低达不到预期的疗效,浓度过高会导致出现不良反应),使药物浓度、药物总吸收量维持在一个合理的水平,从而在获取相应疗效的基础上把不良反应最小化。
据此,为了严格按照方案的要求,高标准、高效率、高质量地完成本研究,并进一步评价“MW33注射液”在健康受试者中单次给药的安全性、耐受性、药代动力学特征和免疫原性,为Ⅱ-Ⅲ期临床试验的顺利开展提供数据支持,经严格筛选,该研究最终共入组42例健康志愿受试者,分5个剂量组进行爬坡试验,即分别按每公斤体重给予4、10、20、40、60 mg的剂量单次注射MW33注射液,其中4 mg剂量组有2名受试者,其余4个剂量组各入组10名受试者。在研究者将MW33注射液后按每公斤体重4、10、20、40、60mg的不同剂量的志愿受试者注射后发现,不同剂量组的受试者其血液内的药物最高浓度、药物总吸收量与给药剂量呈正比,即药物最高浓度、药物总吸收量随着给药剂量的增加成比例增加。此表明MW33注射液在人体内的代谢是有规律的。
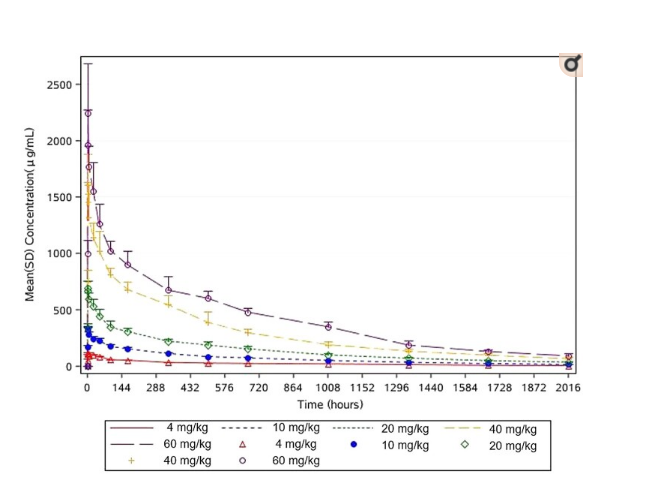
图1 不同剂量组的受试者血液内的药物浓度变化
在药代动力学方面, 4、10、20、40、60mg 5个剂量组其半衰期分别为673.7小时、594.9小时、623.7小时、595.4小时和533.3小时,各剂量组消除速率基本一致,表明人体能用相对恒定的时间把不同剂量的药物代谢排出体外。该结果既让研究者明确了人体何时能把药物排出体外,也方便临床医生有针对性地调整MW33注射液的使用方案。
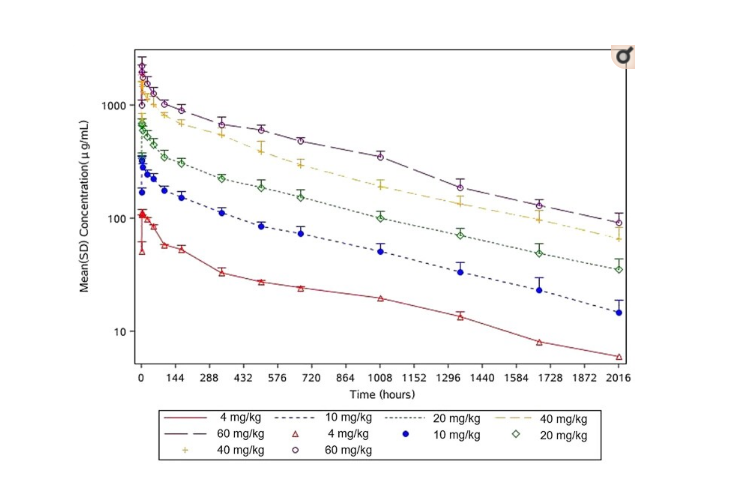
在免疫原性结果方面,共3例受试者6份样本检测为ADA阳性(表示人体内使用某种生物类药物后产生了抗药性抗体),其中2例为试验药物组,均未发生免疫原性与研究药物相关的不良事件。该结果支持MW33注射液进入Ⅱ期临床试验阶段。
卢洪洲教授说,在本试验为期85天的随访过程中, 34例(对照组7例,试验组27例)受试者记录到96例次不良事件。不良事件严重程度除3例次为2级(与研究药物“可能无关”)和1例次为4级(与研究药物“肯定无关”)外,其他92例次严重程度均为1级(最轻)。不良事件是指参与临床试验的受试者在试验过程中发生的任何不良的医学事件。不良事件按严重程度分为5级,比如受试者告知医生说出现鼻塞、流涕、困倦、乏力等,均会被记录为不良事件。虽然记录的不良事件数比较多,但这些不良事件未必与试验药物有关。对于创新药而言,这一发生率及不良事件种类是可以接受的。
据悉,新冠病毒中和抗体是一种治疗性抗体,凭借其特异性和高亲和力特点,能够抢先与新冠病毒刺突蛋白(S蛋白)结合,从而阻断病毒与宿主细胞结合,使病毒无法感染正常细胞,进而被免疫系统清除。从康复患者血液中筛选抗原特异性记忆B细胞克隆,进而克隆获取全人源中和抗体基因,并开发出特异性的中和抗体,是病毒感染性疾病治疗药物开发的重要手段。与康复期患者血浆疗法相比,克隆获取的抗体,质量可控,易于形成规模化,能够更大程度地惠及更多患者。鉴于中和抗体对抗新冠疫情的巨大潜力,从疫情初期即成为国内外各大制药企业研发的重点方向。
通讯员 孙国根
查看更多