查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:复旦大学附属中山医院普通外科 叶博天 住院医师
【病例首诊病情简介】
患者刘凤(化名),女性,65岁,2014年10月因中上部不适3月余就诊于我院。胃镜提示胃角、胃窦巨大溃疡病灶,病理提示低分化腺癌伴坏死。腹盆腔增强CT提示患者胃窦部肿瘤浸润胃壁近全层,胃周淋巴结肿大明显;PET-CT提示未见明确远处转移。术前分期:cT3N+M0。刘女士既往有高血压、糖尿病病史,药物控制良好。按照我院胃癌中心诊疗常规,该病例被提交多学科团队讨论。
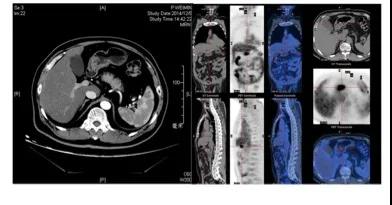
刘女士术前病灶分期:cT3N+M0
本次胃癌病例讨论形成了一致的诊疗方案。与会的多学科专家一致认为,患者胃癌属于局部进展期,手术可根治,如腹腔镜探查无腹膜转移,先行根治性手术,术后再根据病理决定术后治疗方案。

复旦大学附属中山医院 胃肿瘤多学科MDT门诊
参与科室:普通外科、肿瘤内科、影像医学科、病理科、放疗科、介入科等
与患者及其家属充分知情同意后,孙益红教授领衔的外科团队于2014年12月对本例患者施行了标准胃癌根治术(远端胃切除,D2淋巴结清扫,毕I式吻合)。术中腹腔镜探查患者腹腔未见明显种植转移,胃窦小弯侧胃壁增厚,病灶未累及浆膜层,胃周淋巴结可及肿大,与术前临床评估基本一致。术后刘女士在治疗组主管医师汪学非教授团队医护人员的细心照料下,恢复非常顺利,术后第六天即顺利出院。
患者术后病理报告:(远端胃)溃疡型腺癌,分化Ⅱ~Ⅲ级,Lauren分型混合型,浸润胃壁浅肌层。脉管内见癌栓。检出淋巴结共35枚,其中见癌转移5枚。免疫组化:C-MET(80%++),E-cad(+++),EGFR(-),Her-2(2+)。术后病理评估:pT2N2M0,ⅡB期。
经胃癌多学科团队再次讨论,基于2014年胃癌诊疗指南,2015年1月至2015年7月,刘女士接受了六个周期的XELOX方案化疗,化疗期间未出现明显不良反应,此后按期随访复查。
【随访中的第一次新病情】
术后33月起,刘女士逐渐感到腰背部酸痛。复查肿瘤标志物结果显示:CA19-9为112 ng/ml,显著高于正常值;腹盆腔CT提示腹腔内多发淋巴结转移。
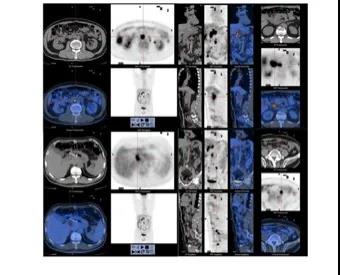
刘女士2017年9月PET-CT:肝门区、胰头旁、腹主动脉旁及左髂血管旁多发淋巴结转移,新增腹盆腔少量积液
获悉刘女士肿瘤复发的消息后,孙益红教授再次建议刘女士至胃肿瘤多学科团队门诊就诊。影像医学科饶圣祥主任仔细比对了患者术前、术后早期和最新的影像学资料,指出目前腹腔内淋巴结转移的病灶已超出根治性手术范围;肿瘤内科刘天舒主任提出,患者目前复发明确存在,除腹腔内多发淋巴结转移,新增腹盆腔积液提示患者可能同时存在腹膜种植转移,综合治疗总体预后较差;放疗科和介入科与会专家亦不主张放疗或介入治疗。讨论最终形成了初步方案:先行姑息一线化疗。随即刘女士开始接受SOX方案化疗。不幸的是,2周期化疗后的影像学疗效评估为较前进展(PD),胃癌多学科团队专家不得不再次坐在一起,共同协商另寻出路。

复旦大学附属中山医院 胃肿瘤多学科MDT门诊 学术讨论
在2017年的彼时,抗PD-1免疫治疗的药物在刚刚美国FDA的批准下对多个癌种获得了适应证,但在中国,抗PD-1药物还只被认为是“颇具潜力”的药物,其疗效还没有得到足够的验证;然而敏锐的复旦大学附属中山医院的胃肿瘤多学科MDT团队发现,2017年8月发表的Attraction-2研究提示,抗PD-1治疗对既往接受过多次化疗的东亚进展期胃癌患者有明显获益。
因此,团队马上联系刘女士,并再次对第一次的外科手术标本进行新的分子诊断,以评估PD-1药物的敏感性。
我们欣喜地发现,患者标本的检测结果显示为“微卫星不稳定(MSI-H)”类型。肿瘤内科刘天舒主任告诉患者,抗PD-1药物可能会让刘女士的病情有所好转。
2018年2月刘女士第一次接受抗PD-1治疗。首次用药一周后刘女士的腰背痛即明显好转;用药2月后的复查结果提示腹腔内淋巴结较前明显缩小,肿瘤标志物CA19-9明显降低。
此后,刘女士持续接受PD-1抗体免疫治疗24个月,用药后没有明显的免疫治疗相关不良反应。多次影像学检查显示复发肿瘤已消失。患者一般情况良好,营养摄入良好,体重亦恢复至手术前水平。
【随访中的第二次新病情】
2019年5月刘女士的CT检查结果显示,胰头旁、腹主动脉旁两处淋巴结相比于之前,再次增大了。同时,肿瘤标志物CA19-9亦再次升至55 ng/ml。但与第一次复发不同的是,患者全身情况良好,无相关不适主诉,饮食、营养状况均无改变。
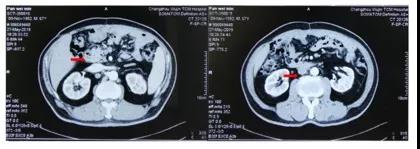
图5 刘女士2019年5月CT:胰头旁、腹主动脉旁淋巴结肿大,较前进展
在与肿瘤抗争了近5年之后,刘女士已经完全从当年的“谈癌色变”的恐慌状态中走了出来,再次面对复旦大学附属中山医院胃癌中心多学科团队的诸位专家,刘女士显得非常坦然。
本次多学科讨论中,普外科汪学非主任医师提出了联合用药的可能性。阿帕替尼是全球第一个在晚期胃癌被证实安全有效的小分子抗血管生成靶向药物,也是晚期胃癌标准化疗失败后,明显延长生存期的单药;同时,复旦大学附属中山医院一项阿帕替尼联合Xeloex方案化疗在伴有融合淋巴结转移的进展期胃癌中应用的研究亦有了非常欣喜的结果。而刚刚在2019年1月,一项阿帕替尼联合抗PD-1治疗在进展期肝细胞肝癌、胃癌和食管胃连接处腺癌的临床研究结果崭新出炉,联合用药的不良反应尚可接受。在胃肿瘤多学科团队的建议下,刘女士接受了小剂量阿帕替尼靶向治疗+抗PD-1免疫治疗的方案。
命运女神再一次垂青了刘女士,小剂量阿帕替尼联合PD-1治疗后3个月,影像学复查结果显示,原来增大的复发肿瘤再一次缩小了。2020年5月,增强CT检查,复发肿瘤再次完全消失。目前,刘女士仍在服用小剂量阿帕替尼,联合应用PD-1抗体免疫治疗。我们会持续跟踪患者病情变化。

图6 刘女士2019年12月CT:胃MT综合治疗后,腹腔淋巴结较前明显缩小
手术、化疗、免疫治疗、联合靶向治疗。在刘女士的身上,我们看到了多种多样的胃癌治疗手段,而每一种治疗手段都在合适的时期内极大地改善了刘女士的肿瘤情况,达到了从手段到结果的统一。复旦大学附属中山医院胃癌中心,在孙益红教授的带领下,始终坚持规范化、个体化的诊疗原则,时刻更新世界范围内的最新研究进展,与时俱进,并结合患者自身情况选择最佳治疗方案。到目前为止,胃癌仍然是我国最为高发和高死亡率的肿瘤性疾病之一,但有信心的是,面对胃癌,我们手上的武器正越来越多,消灭和控制肿瘤的机会也越来越大。医患一心同归,我们共同期待着科学家攻克胃癌的那一天早日来临。
来源:复旦大学中山医院肿瘤防治中心

查看更多