查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





免疫效应细胞相关神经毒性综合征(ICANS)是嵌合抗原受体T细胞(CAR-T)治疗后可能出现的一种严重并发症。随着CAR-T疗法在恶性血液肿瘤治疗中的广泛应用,这种神经系统毒性反应引起了临床医生的高度关注。根据近期 J Neurol Neurosurg Psychiatry 杂志发表的综述,本文将从ICANS的临床特点、诊断与分级、鉴别诊断以及病理生理机制等方面进行解读,以期为临床实践提供参考。
ICANS的临床表现多种多样,典型症状通常在CAR-T细胞输注后5天左右出现,并在第7-8天达到峰值。大多数病例在适当治疗后两周内可完全缓解,但少数患者可能出现延迟性发作(输注后3周以上)或症状持续、难治的情况。症状通常在数小时至数天内逐渐发展,罕见情况下可呈现类似血管事件的急性发作。脑病是ICANS最常见的临床表现,患者可能出现意识状态改变,从轻度嗜睡到昏迷不等。值得注意的是,即使在严重ICANS病例中,患者的警觉性可能保持相对完好。
语言障碍和书写困难是ICANS的特征性表现。表达性失语伴语言流利度降低、词汇查找困难和说错话是ICANS最特异的临床特征之一。在严重病例中,失语可能进展为全面性失语,甚至导致运动性缄默。书写障碍可能是ICANS的早期甚至是孤立表现,从拼写或字形错误到完全无法书写不等。这些语言和书写障碍往往为神经系统受累提供了重要线索,特别是在患者没有其他明显神经系统症状的情况下。
ICANS还可表现为多种皮质性体征和高级功能障碍,包括观念运动性失用、计算困难和记忆障碍。癫痫发作在1%-30%的ICANS病例中被报道,以强直-阵挛发作最为常见,偶尔可表现为明显的局灶性起始,较少见的是非惊厥性癫痫持续状态,后者可能被漏诊。最严重且危及生命的ICANS直接并发症是脑水肿,影响1%-2%的治疗患者,可从看似轻微的初始神经系统症状迅速发展。脑水肿在CD19靶向CAR-T产品治疗中更为常见。其他在ICANS背景下报道的死亡原因包括弥散性血管内凝血(DIC)背景下的出血和皮质层状坏死。
在ICANS诊断方面,免疫效应细胞相关脑病(ICE)评分是临床评估的基础。这是一个10分量表,包含定向力、命名、书写、注意力和执行命令能力的测试。ICE评分被整合到美国移植和细胞治疗协会共识组定义的整体神经功能分级中,该分级还包括意识状态、癫痫发作、运动无力和影像特征的评估。ICANS严重程度通常被二分为低级别(1-2级)和高级别(≥3级)。

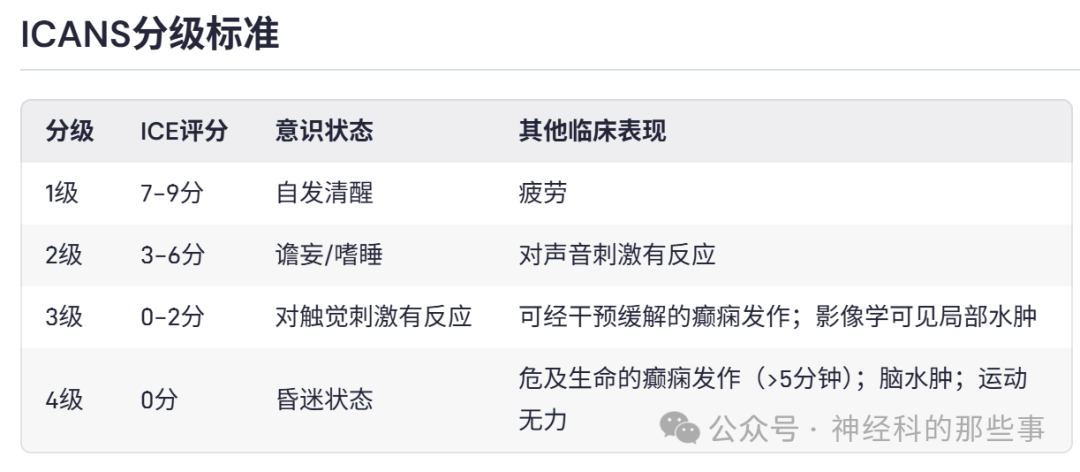
虽然ICE评分设计用于血液学/肿瘤学医生在床旁快速评估,但它既不敏感也不特异。ICANS引起的认知缺陷可能并不总是被ICE评分捕捉到,而ICE评分的降低也并不总是反映ICANS。这种特异性缺乏可能导致在面对ICANS广泛鉴别诊断时采取不适当的治疗措施。
鉴别诊断是ICANS管理中的重要环节。在CAR-T治疗后,患者面临几种可能模仿ICANS的神经系统疾病风险。诊断挑战因ICANS表现多样而加剧。脓毒症相关脑病、谵妄和类固醇诱导的精神病均可类似ICANS。在这些情况下使用免疫抑制治疗可能加重这些疾病。因此,特别是在长期或明显类固醇难治性ICANS的情况下,排除鉴别诊断尤为重要。
患者在CAR-T治疗后免疫抑制严重,感染性脑炎风险较高。有报道称人类疱疹病毒6型、巨细胞病毒和JC病毒的病毒重活化,后者可引发进行性多灶性白质脑病。急性发作的ICANS可能模仿癫痫发作或缺血性卒中,特别是当语言缺陷显著时。患者也更容易发生脑出血,特别是在CAR-T相关血小板减少的情况下。在CAR-T前使用氟达拉滨进行淋巴细胞消除可能导致延迟性氟达拉滨相关白质脑病,临床上可能类似ICANS。在这种情况下,影像学检查很有帮助,因为氟达拉滨主要影响白质,在MRI上表现为明显的改变。最后,涉及中枢神经系统的恶性肿瘤复发可能导致类似ICANS的症状。
ICANS的病理生理机制尚未完全阐明,但大体上是一种大脑半球的炎症过程,对特定脑结构有偏好,这从语言和书写的特征性缺陷可见一斑。ICANS很少在没有先前细胞因子释放综合征(CRS)的情况下发生,而早期或更严重的CRS与更高级别的ICANS相关。这些观察将CRS纳入ICANS病理生理模型中:CRS期间血管内皮和血脑屏障(BBB)的变化可能允许CAR-T细胞、其他炎症介质和内源性免疫细胞浸润到中枢神经系统,导致神经系统症状,严重情况下甚至引起脑水肿。
ICANS背景下出现脑水肿的患者常表现出CAR-T细胞的快速、早期扩增,伴随细胞因子水平上升和血脑屏障的完全破坏,在尸检中表现为血管壁破坏和多灶性出血。在输注CAR-T后7天测量的血管生成素2(ANG2)与ANG1比率(内皮激活和毛细血管渗漏的标记物)在严重ICANS患者中升高。内皮损伤和DIC,包括凝血酶原时间延长、活化部分凝血活酶时间延长、D-二聚体升高以及蛋白质和白蛋白降低,也在ICANS中被报道。
血清干扰素γ(IFNγ)水平升高与ICANS相关,IFNγ促进T细胞穿过血脑屏障迁移。脑脊液蛋白升高和MRI上偶有对比增强的病例均进一步支持ICANS中血脑屏障破坏和内皮激活的模型。然而,血脑屏障破坏并不能解释ICANS的所有方面,特别是失语和失用等明显局灶性神经系统特征。
一些研究发现ICANS与低磷血症有相似之处,而低磷血症是一种独立的风险因素。低磷血症可能通过干扰能量代谢、膜稳定性和神经递质功能来影响神经系统。一项小型研究表明,纠正低磷血症可能有助于减轻ICANS症状。
ICANS的风险因素研究表明,年龄是最一致的风险因素,60岁以上患者ICANS风险显著增加。这可能与老年人血脑屏障完整性降低有关。体重也被确定为风险因素,体重指数较高与更严重的ICANS相关。输注前肿瘤负荷或其替代指标乳酸脱氢酶(LDH)在一些但非所有病例中被发现是ICANS的风险因素。组织学肿瘤亚型也可能与ICANS相关。
预先存在的神经系统疾病经常被报道为发展ICANS的危险因素。在一项纳入16例患者的小型系列研究中,只有那些基线时被发现有微小额叶缺陷的患者后来发展为ICANS,表现为额叶受累(语言障碍和额叶起源的皮质肌阵挛)。输注前其他指标也可能指示发展ICANS的风险,包括较低的血小板计数、高纤维蛋白原、较高的CRP、增加的ANG2:ANG1比率以及细胞因子IL-6、IL-10、IP-10、G-CSF和GM-CSF水平升高。
总而言之,ICANS是CAR-T治疗后一种重要的神经系统毒性反应,临床表现多样,以脑病、语言障碍和书写困难为特征。ICE评分作为诊断和分级的基础工具,虽有局限性但在临床实践中广泛应用。鉴别诊断复杂,需排除感染、卒中、出血等多种可能。病理生理机制涉及血脑屏障破坏、内皮激活、细胞因子风暴等多种因素。随着CAR-T疗法的广泛应用,深入理解ICANS的临床特点、诊断方法、鉴别诊断策略和病理生理机制对于早期识别、及时干预和改善患者预后至关重要。
当前,CAR-T细胞疗法已从血液系统肿瘤逐步扩展到实体瘤甚至自身免疫疾病(如多发性硬化、重症肌无力、系统性红斑狼疮等)的临床试验领域。目前ICANS在CAR T细胞治疗自身免疫性疾病时出现的概率相对较低,但仍需进一步积累临床安全性数据予以支撑。
免疫效应细胞相关神经毒性综合征(ICANS)的影像学表现多样,值得注意的是,即使在严重ICANS病例中,许多患者的影像学检查也可能完全正常。然而,随着ICANS严重程度增加,影像学改变的可能性也随之增大。磁共振成像(MRI)是ICANS诊断中最有价值的影像学工具,显示了多种特征性改变。最常见的MRI表现是双侧丘脑的可逆性T2/FLAIR高信号和肿胀,有时这些改变延伸至其他深部结构,包括基底节、外囊、海马和脑干。尽管这些表现较为典型,但它们缺乏特异性。大多数情况下,弥散受限并不明显,但当存在时,往往涉及半卵圆中心白质和胼胝体。其他MRI发现包括幕上白质的T2高信号、皮质或白质中局灶性的类似卒中区域,以及通常弥漫但可能斑片状的脑膜增强。
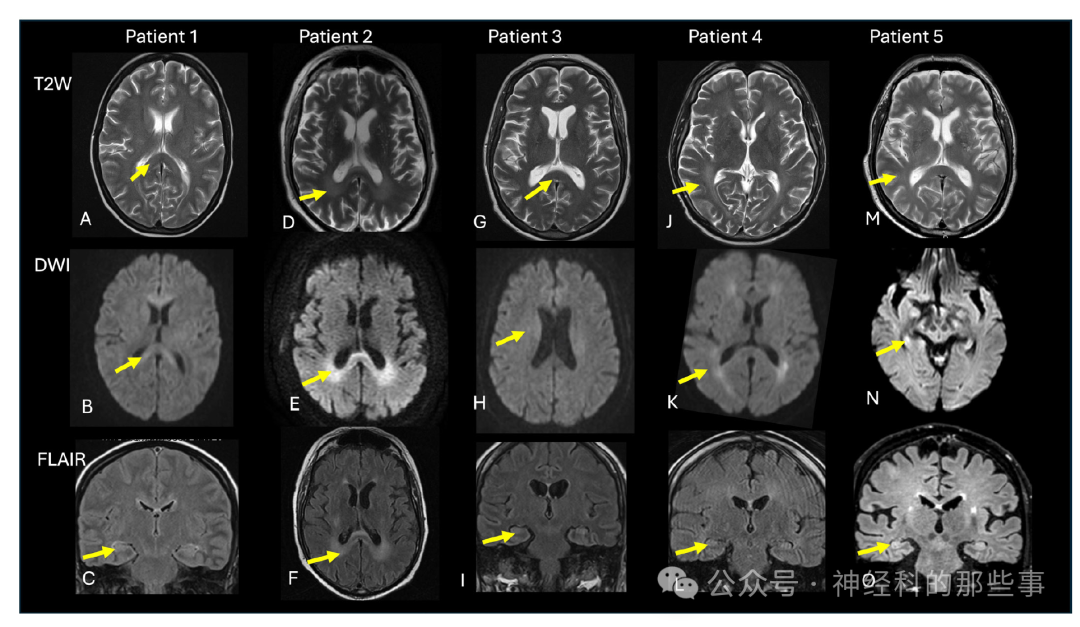
图:患者1:(A)轴位T2加权成像显示双侧幕上深部白质弥漫性信号异常,(B)与胼胝体受限弥散有关,并且每侧海马均可见信号异常(C)。患者2:轴位T2加权成像显示脑室周围及胼胝体压部弥漫性信号异常(D),与受限弥散(E)相关,FLAIR(F)予以确认。患者3:轴位T2加权成像(G)显示隐匿的幕上白质信号异常,也累及胼胝体压部,(H)与轻度幕上受限弥散相关,并于FLAIR(I)中可见双侧海马信号异常。患者4:轴位T2加权成像(J)显示弥漫性幕上信号异常,伴脑室周围受限弥散(K),FLAIR(L)予以确认,也累及双侧海马。患者5:轴位T2加权成像(M)显示弥漫性幕上信号异常,(N)DWI显示双侧海马体受限弥散,(O)每侧海马信号异常。DWI:弥散加权成像;FLAIR:液体衰减反转恢复成像;T2W:T2加权成像。
在癫痫发作相关的ICANS病例中,典型的影像学改变包括双侧海马的异常信号和弥散受限。少数文献报道了胼胝体的细胞毒性病变或胼胝体内的点状炎性病变。计算机断层扫描(CT)虽然敏感性较低,但在检测与内皮功能障碍或血小板减少相关的颅内出血方面仍有价值。CT或MR血管造影在某些ICANS病例中可显示血管痉挛,但受累血管与临床综合征之间通常缺乏相关性。
高级影像学技术,如弥散张量成像和功能性MRI,虽然研究样本有限,但为理解ICANS的病理生理机制提供了宝贵线索。弥散张量技术显示胼胝体体部和压部的部分各向异性降低,提示神经纤维束完整性受损。功能性MRI研究发现ICANS患者的功能连接存在中断,且这种中断在Broca区和Wernicke区(语言优势半球)最为严重,这可能解释了ICANS中经常观察到的语言障碍。正电子发射断层扫描(PET)的结果虽不一致,但最常见的是显示全脑弥漫性代谢减低,有时以额叶为主,或涉及其他皮质区域或一侧脑区。
ICANS的生物标记物研究为理解其发病机制和预测疾病风险提供了重要依据。细胞因子的检测是ICANS评估的核心,多项研究表明,与细胞因子释放综合征(CRS)相关的细胞因子水平升高是ICANS发展的重要风险因素。血清中干扰素γ(IFNγ)水平升高与ICANS显著相关,IFNγ促进T细胞穿过血脑屏障迁移,这可能是ICANS发病的关键机制之一。其他与ICANS相关的细胞因子包括IL-6、IL-10、IL-1RA、GM-CSF和IP-10。
内皮激活标志物也是ICANS的重要生物标记。CAR-T细胞输注后7天测量的血管生成素2(ANG2)与ANG1比率在严重ICANS患者中明显升高,这一指标反映了内皮活化和毛细血管渗漏。修饰的内皮激活和应激指数(m-EASIX)分数作为内皮破坏的衡量标准,也被证明可预测ICANS严重程度。血清中新型生物标记物如神经丝轻链(NfL)的升高预示着任何级别的ICANS风险,特别是重度ICANS的发生。此外,胶质纤维酸性蛋白(GFAP)和S100B的升高支持了ICANS发病机制中胶质细胞功能障碍的可能性。
脑脊液检查在ICANS诊断中具有重要价值,尤其是排除可能混淆ICANS的疾病,如感染性脑炎等。ICANS患者的脑脊液中白细胞通常轻度升高,但与疾病严重程度不相关。蛋白质含量可能显著增加,且与ICANS严重程度呈正相关。CAR-T细胞在输注后经常能在脑脊液中被检测到,但其水平与ICANS严重程度的相关性在不同研究中结果不一。一些证据表明,多种在ICANS期间在脑脊液中发现的细胞因子源自血液,通过血脑屏障破坏进入鞘内,但也有研究支持IL8、IP10和MCP1可能在鞘内局部产生。
脑电图(EEG)在ICANS诊断和评估中具有不可替代的作用。ICANS患者的EEG通常表现异常,最常见的非特异性发现是弥漫性或以额叶为主的背景节律减慢,这可能与ICANS严重程度相关,或表现为全脑性节律性δ活动。其他常见表现包括后部优势节律消失。在重度ICANS中,EEG可显示处于癫痫发作-间歇连续状态【是脑电活动从“发作前(间歇期,interictal)”到“典型癫痫发作(ictal)”之间的一个连续谱。这类EEG表现介于正常脑电、典型癫痫发作和完全恢复之间】的特征,特别是广泛性周期性放电(GPDs),这可能与临床严重程度相关。非惊厥性癫痫持续状态(NCSE)在ICANS中较为罕见,但EEG在此严重并发症的诊断中起着关键作用。
一些研究表明,局灶性减慢、侧化的周期性放电(LPDs)和侧化的节律性δ活动(LRDA)可能与局灶性临床缺陷(特别是语言缺陷)相关。然而,这些发现并不一致,定量化的自动EEG分析未能发现ICANS与LPD或LRDA之间的显著关联。此外,在具有局灶性EEG异常的患者中,FDG-PET显示相应区域代谢减低,这与局灶性癫痫活动通常表现出的代谢增高形成对比。虽然EEG在指导ICANS管理方面的作用尚未完全阐明,但缺乏癫痫发作-间歇连续状态特征是ICANS的强有力的阴性预测因子。
ICANS的处理措施应基于全面的评估和分级。对于低级别ICANS(1-2级),通常采取支持性治疗和密切监测。维持患者安全、防止坠床、监测液体和电解质平衡以及营养支持是基础措施。许多中心通常为这些患者常规使用抗癫痫药物(主要是左乙拉西坦)作为预防性措施,但这一做法的循证支持有限。在神经症状出现前使用的药物称为初级预防,而在CRS或早期神经症状出现时使用则称为预先预防。
对于高级别ICANS(≥3级),除了支持性措施外,还应考虑使用皮质类固醇。地塞米松是首选药物,初始剂量为10mg,然后每6小时给予10mg,直至症状改善。在严重或进行性神经系统症状的情况下,可能需要更高剂量或甲泼尼龙冲击治疗。值得注意的是,皮质类固醇使用应权衡抑制CAR-T细胞活性的风险。托珠单抗(IL-6受体拮抗剂)作为CRS的主要治疗药物,在单独ICANS的管理中作用有限,但对于同时存在CRS和ICANS的患者可能有益。
对于顽固性或治疗难治性ICANS,可能需要考虑其他免疫抑制策略,如环孢素、他克莫司、阿那白滞素(anakinra,IL-1拮抗剂)或西罗莫司(mTOR抑制剂)。然而,这些药物的使用经验有限,应谨慎个体化选择。对于罕见但危及生命的脑水肿,除了积极的药物治疗外,可能需要神经外科干预,如脑室外引流以控制颅内压。
癫痫发作是ICANS的常见并发症,应迅速处理。对于临床癫痫发作,苯二氮卓类药物(如劳拉西泮)是一线治疗选择,随后可使用左乙拉西坦等抗癫痫药物持续治疗。对于疑似非惊厥性癫痫持续状态,应在神经科医师指导下进行EEG监测和治疗。此外,对于出现精神状态变化的患者,应排除可能的代谢异常、感染和药物相互作用等因素。
ICANS的预防措施主要基于风险评估和早期干预。年龄是最一致的风险因素,60岁以上患者ICANS风险显著增加,这可能与老年人血脑屏障完整性降低有关。对这些高风险患者,应考虑更密切的监测和更积极的预防性措施。体重和体质指数(BMI)也是已确认的风险因素,较高的体质指数与更严重的ICANS相关。然而,肌肉量减少也预示ICANS的发展,这表明虚弱可能是一个独立的风险因素。
细胞因子释放综合征(CRS)的存在、时间和严重程度是ICANS的最重要预测因子。几乎所有研究都表明,早期或严重的CRS预示更严重的ICANS。CRS与ICANS之间的关联可能解释了输注后早期几天内预测ICANS的几个指标,包括低血小板、温度升高、CRP、铁蛋白、IL-6和降钙素原升高。事实上,预测严重CRS的预后评分也能预测严重ICANS的发展。CAR-T细胞在体内的扩增速率和程度也是ICANS发展的公认风险因素。
基于对这些风险因素的理解,一些预防性策略已经被提出并部分实施。首先,优化CAR-T产品和给药策略是减少ICANS风险的重要途径。使用非CD28内结构域的CAR-T产品(如tisa-cel和liso-cel)可能降低ICANS的发生率和严重程度。其次,对高风险患者,特别是老年人、体重指数较高或有既往神经系统疾病史的患者,应考虑在CAR-T输注前采取预防性措施,如提前使用抗癫痫药物。
在CAR-T输注期间,严密监测CRS的发展和早期识别神经系统症状至关重要。应定期评估患者的神经状态,包括ICE评分、语言功能、书写能力和意识水平。对于出现早期CRS或其他ICANS风险因素的患者,可考虑早期干预,包括低剂量皮质类固醇或在适当情况下使用托珠单抗。
此外,维持患者的电解质平衡,特别是纠正低磷血症,可能有助于减轻ICANS症状。有研究表明,ICANS与低磷血症有相似之处,而低磷血症是一种独立的风险因素。低磷血症可能通过干扰能量代谢、膜稳定性和神经递质功能来影响神经系统。
随着CAR-T治疗在恶性肿瘤甚至自身免疫性疾病治疗中的应用不断扩大,深入理解ICANS的这些方面将有助于优化患者预后和降低治疗相关风险。未来的研究应继续探索ICANS的发病机制,开发更精准的预测模型和更有效的预防策略,同时关注新型CAR-T产品和新适应证下ICANS的表现特点和管理策略,为个体化治疗提供更坚实的科学基础。

来源:神经科的那些事
查看更多