查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过







癌细胞的有丝分裂周期分为5个阶段:静止期G0、DNA合成前期G1、DNA合成期S、DNA合成后期G2、分裂期M,这些不同阶段受到不同的周期蛋白控制。
其中,周期蛋白D1负责控制G1期进入S期。在雌激素和雌激素受体的过度刺激下,周期蛋白D1与周期蛋白依赖性激酶CDK4和CDK6结合,将抑癌蛋白Rb磷酸化而失去抑癌作用,导致癌细胞由G1期进入S期失控,从而陷入疯狂复制的死循环。
对于内分泌治疗耐药的激素受体阳性乳腺癌患者,CDK4和CDK6抑制剂可有效阻断这个死循环。
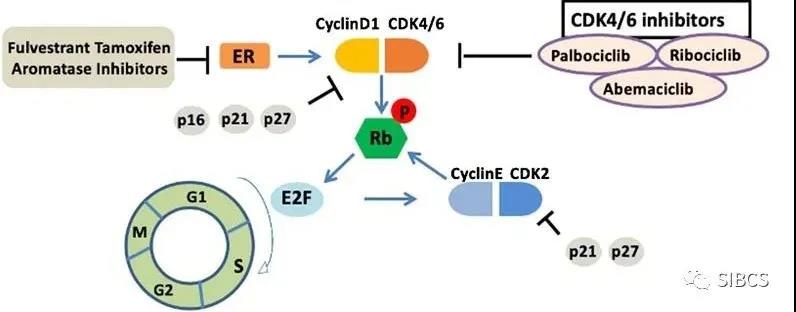
目前,已有三种CDK抑制剂(哌柏西利、阿贝西利、瑞博西利)被批准联合内分泌治疗用于激素受体阳性HER2阴性晚期乳腺癌患者的一线或二线治疗。
2019年,英国《柳叶刀》肿瘤学分册(The Lancet Onco)发表美国食品药品监督管理局(FDA)的研究报告,对CDK抑制剂联合内分泌治疗用于激素受体阳性HER2阴性晚期乳腺癌患者的无进展生存(PFS)期结局进行了汇总分析,结果表明,全部重要的临床病理亚组都能获益。随着越来越多的临床研究已经公布总生存(OS)结局,故有必要对OS结局进行汇总分析。
2021年10月14日,英国《柳叶刀》肿瘤学分册在线发表FDA药品审评研究中心的研究报告,首次对CDK抑制剂联合雌激素受体降解剂氟维司群治疗激素受体阳性HER2阴性晚期乳腺癌患者的总生存结局进行了汇总分析。
该探索性分析对2020年8月1日前提交并获得美国食品药品监督管理局批准上市的CDK抑制剂或安慰剂联合氟维司群治疗乳腺癌随机对照Ⅲ期临床研究患者个体数据进行汇总分析:
MONARCH-2研究:阿贝西利+氟维司群一线或二线治疗(713例)
PALOMA-3研究:哌柏西利+氟维司群二线治疗(521例)
MONALEESA-3研究:瑞博西利+氟维司群一线或二线治疗(726例)
全部被分析的患者年龄≥18岁,美国东部肿瘤学协作组体力状态评分为0~1,激素受体阳性HER2阴性晚期乳腺癌,并接受至少一次CDK4抑制剂或安慰剂联合氟维司群。
通过生存曲线推算中位OS期,通过多因素比例风险回归模型推算不同因素的总死亡风险比及其95%置信区间(CI)。对既往全身内分泌治疗线数(一线或内分泌初治与二线及以上)以及不同的临床病理特征亚组进行汇总比较。
由于潜在患者异质性,当汇总人群包括跨线治疗患者时,未按组报告推算中位OS期。全部结果为探索性和假设生成。
结果,3项研究合计1960例患者于2013年10月7日~2016年6月10日被随机分组,其中12例患者未治疗、1296例(66%)患者被随机分入CDK抑制剂组、652例(33%)被随机分入安慰剂组。
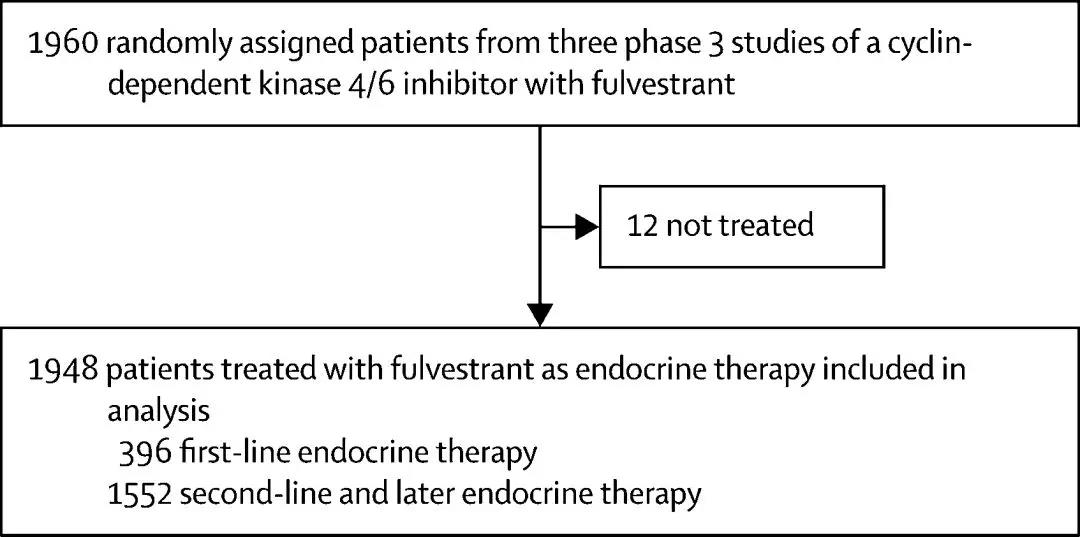
对于接受治疗的全部1948例患者,中位随访43.7个月(四分位:37.8~47.7)期间死亡935例(48%),CDK抑制剂组与安慰剂组相比:
总死亡风险减少23%(推算风险比:0.77,95%置信区间:0.68~0.88)
中位OS期延长7.1个月(范围:7.0~10.6个月)
对于其中2项研究的396例一线治疗患者,中位随访39.4个月(四分位:37.0~42.2个月)期间死亡123例(31%),CDK抑制剂组与安慰剂组相比:
总死亡风险减少26%(推算风险比:0.74,95%CI:0.52~1.07)
中位总生存期未达到终点(未达到 对45.7个月,95%CI:50.9个月~未达到、41.7个月~未达到)
对于其中3项研究的1552例二线治疗患者,中位随访45.1个月(95%CI:39.2~48.5个月)期间死亡812例(52%),CDK抑制剂组与安慰剂组相比:
总死亡风险减少23%(推算风险比:0.77,95%CI:0.67~0.89个月)
中位OS期延长7.0个月(范围:7.0~9.5)
对于其他临床病理特征亚组,除了年轻亚组、亚裔亚组、初诊转移亚组,氟维司群+CDK抑制剂与氟维司群+安慰剂相比,OS获益一致。
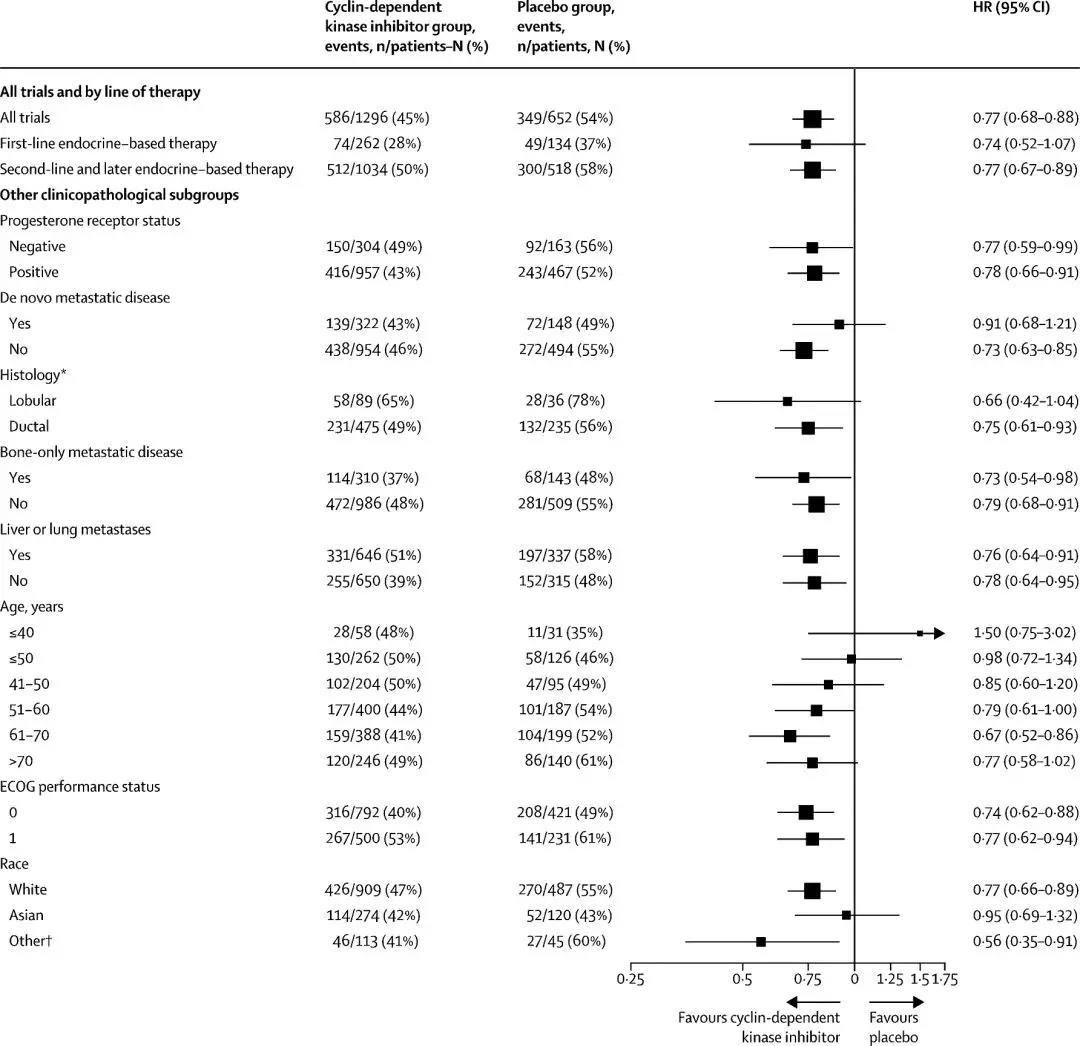
因此,该研究结果表明,对于全部汇总患者和大多数临床病理特征亚组,氟维司群+CDK抑制剂与氟维司群+安慰剂相比,都可OS获益。这些结果支持CDK抑制剂+氟维司群治疗激素受体阳性/HER2阴性晚期乳腺癌患者的现有治疗标准。
SIBCS 平台发布
查看更多