查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2021年欧洲肿瘤内科学会(ESMO)年会于2021年9月16-21日线上召开。前列腺癌作为男性泌尿生殖系常见的恶性肿瘤,备受参会专家关注。转移性去势抵抗性前列腺癌(mCRPC)既是前列腺癌治疗的难点,也是当下创新药物研发的焦点。为此,我们对会议内容做了检索及研究解读,以深入了解mCRPC免疫治疗的最新进展。
KEYNOTE-365是一项开放标签、多中心、多队列、非随机化的Ib/II期研究,旨在评估帕博利珠单抗(Pembro)固定剂量联合多种药物治疗mCRPC的疗效和安全性。KEYNOTE-199是一项多中心开放标签、多队列的II期研究,主要探索帕博利珠单抗在新型内分泌经治或多西他赛经治的mCRPC患者中的抗肿瘤活性及安全性。下面内容主要解析KEYNOTE-365队列A和KEYNOTE-199队列4和5的最新研究成果。
Keynote-365队列A:Pembro联合奥拉帕利治疗多西他赛经治mCRPC患者的11个月以上的随访数据更新[1]
【Abstract 612P】
KEYNOTE-365(NCT02861573)队列A纳入124例多西他赛经治、未经分子选择的mCRPC患者,进行Pembro静脉注射(200mg Q3W)联合奥拉帕利口服(300 mg片剂/400 mg胶囊BID)干预,随访11.4个月的时间,观察Pembro联合奥拉帕利治疗mCRPC患者的疗效。研究主要终点为前列腺癌肿瘤标志物(PSA)应答率(比基线下降≥50%)、客观缓解率(ORR)(RECIST v1.1 by BICR)和安全性,次要终点为疾病控制率(DCR)(完全缓解(CR)或部分缓解(PR)+疾病稳定(SD)或非CR/非疾病进展(PD)≥6个月、中位缓解持续时间(DOR)、无影像学进展生存期(rPFS)(PCWG-3)和总生存期(OS)。
在104例入组患者中,102例患者进行了治疗。研究的中位随访时间(定义为从入组到数据截止时间)为19.3个月(11.4-45.9个月)。经基线评估的患者的PSA应答率为14.7%(N=102)(95%CI,8.5-23.1)(图1)。在58例可评估疾病的患者中,ORR为6.9%(95%CI, 1.9-16.7;4PRs)。整个研究中,患者未达到中位DOR(7.2+-37.8+个月),其中2例患者反应时间≥12个月。研究中DCR为26.5% (95%CI,18.2-36.1)。中位rPFS为5.2个月(95% CI, 4.1-6.5),12个月的rPFS率为28.8%(图2)。中位OS为14.4个月(95% CI,10.4-17.9),12个月OS率为55.9%(图3)。93例患者(91.2%)发生治疗相关的不良事件,最常见的是贫血(41.2%)、恶心(41.2%)、食欲下降(30.4%)和乏力(30.4%),3-5级不良事件发生49例(48.0%)。整项研究死亡6例(5.9%),其中2例死亡与治疗相关(原因不明和心肌梗死)。
综上所述,基于11.4个月的随访,Pembro联合奥拉帕利治疗多西他赛经治、未经分子选择的mCRPC患者中表现出了适度的抗肿瘤活性和可接受的安全性。
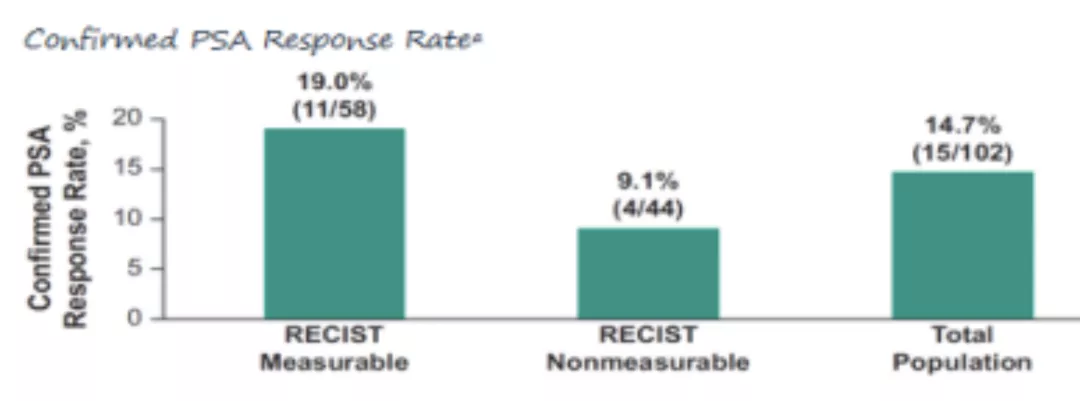 图1
图1
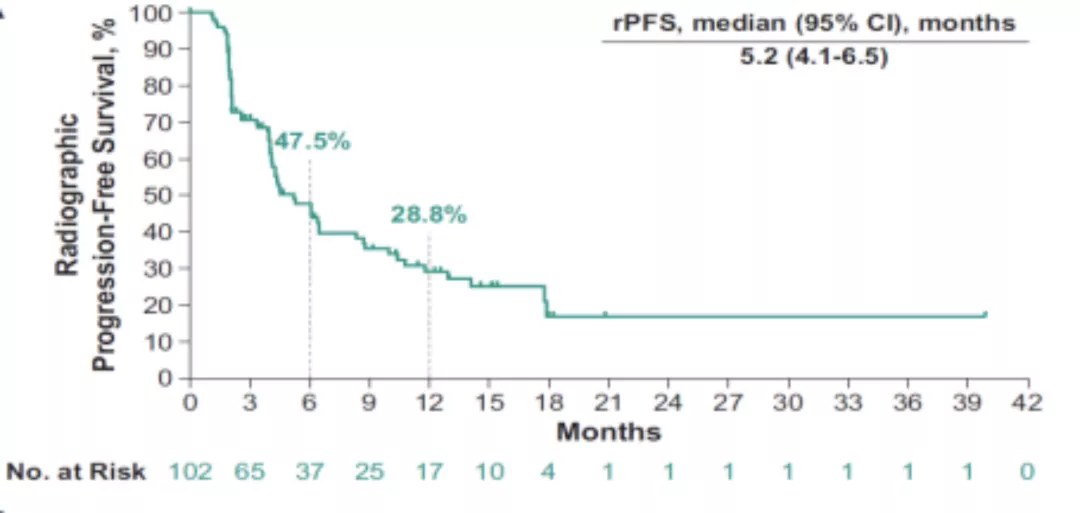 图2
图2
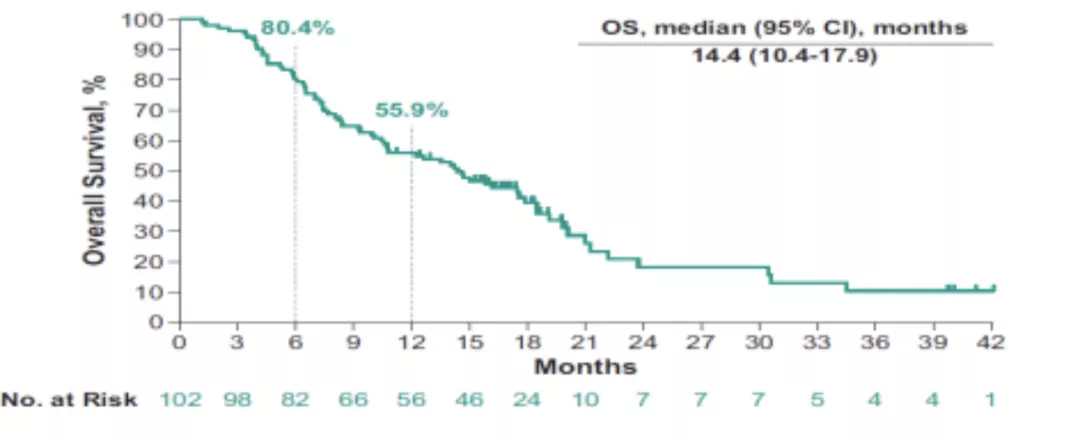 图3
图3
KEYNOTE-365队列A:Pembro联合奥拉帕利治疗mCRPC的生物标志物分析[2]
【Abstract 73P】
mCRPC中发现同源重组修复基因突变(HRRm)(如BRCAm)与PARP1抑制剂(如奥拉帕利)的应答相关。KEYNOTE-365(NCT02861573)队列A纳入124例多西他赛经治、未经分子选择的mCRPC患者,进行Pembro联合奥拉帕利干预,评估了BRCAm和HRRm的发生率及其与抗肿瘤活性的关系。
研究采用PSA应答率和ORR评估抗肿瘤活性,采用FoundationOne®CDx(F1CDx)进行FFPE组织分析。ctDNA(GH360或GH Omni)检测结果显示,BRCAm阳性为3/98例(3%),HRRm阳性为14/59例(24%,GH Omni);F1CDx检测结果显示,BRCAm阳性和HRRm阳性分别为4/41例(10%)和12/41例(29%),研究发现GH ctDNA检测和F1CDx检测BRCA(98%一致性)和HRR(87%一致性)突变状态之间具有高度一致性。在PSA应答率方面,BRCAm组患者的PSA应答率为50%[2/4 (95%CI,6.8%-93.2%)],非BRCAm患者的PSA应答率为14%[13/95(7.5%-22.3%)];HRRm组患者PSA应答率为22%(4/18[6.4%-47.6%)],非HRRm组患者PSA应答率为13%[7/52(5.6%-25.8%])。在RECIST可评估患者(N=58)中,BRCAm组ORR为33%[1/3(0.8%-90.6%)],非BRCAm组ORR为6%[3/53(1.2%-15.7%)];HRRm组ORR为8%[1/12(0.2%~38.5%)],非HRRm组ORR为3%[1/30(0.1%-17.2%)]。
综上所述,GH ctDNA与F1CDx在检测BRCAm和HRRm突变状态方面具有高度一致性,BRCAm、HRRm患者的PSA应答率和ORR也高于非BRCAm、HRRm的患者。然而,与Pembro单药或奥拉帕利单药治疗相比,不论HRRm结果如何,Pembro联合奥拉帕利均可以提高PSA应答率。鉴于样本量较小,数据还需谨慎解读。
KEYNOTE-199队列4和5(C4-C5):Pembro联合恩扎卢胺治疗恩扎卢胺耐药mCRPC患者的生物标志物分析[3]
【Abstract: 61MO】
KEYNOTE-199(NCT02787005)的C4-C5主要研究帕博利珠单抗联合恩扎卢胺治疗恩扎卢胺耐药的mCRPC患者的疗效,本次报道从生物标志物角度进行分析,评估了预先指定的生物标志物与临床结果之间的关联性。
队列4纳入81例患者(C4纳入RECIST-可评估的疾病),队列5纳入45例患者(C5纳入以骨转移为主、不可评估的疾病)。分组后患者接受Pembro静脉注射(200 mg Q3W)联合恩扎卢胺口服治疗(160 mg QD),直至疾病进展或出现无法耐受的毒性终止。研究采用全外显子测序法评估肿瘤突变负荷(TMB)(N=64),IHC法评估PD-L1综合阳性评分(CPS)(N=124),NanoString法评估18种T细胞炎症基因表达谱(TcellinfGEP)(N=51),以分析这些生物标志物与疗效结局[DCR、PFS、PSA应答、PSA进展、OS、ORR(仅C4)]之间的关联。
在C4中,具有TMB数据的患者ORR为10%(5/48),具有CPS数据的患者ORR为12%(10/81)(表1)。在C4和C5中,TMB和CPS数据显示,分别有16%(10/64)和14%(17/124)的患者出现PSA应答(表1)。研究发现TMB与DCR呈显著相关(P=0.03),且与PSA应答呈正相关(P=0.08)(表1)。TMB、CPS和TcellinfGEP与PFS或OS无关,当TMB≥175 mut/exome(11%)和高TcellinfGEP时,Pembro联合恩扎卢胺治疗改善了结果(≥-0.318,16%)。
KEYNOTE-199的C4-C5中,PD-L1 CPS和TcellinfGEP没有显示与Pembro联合恩扎卢胺临床结局相关的证据。尽管TMB ≥ 175 mut/exome 的比率较低,TMB与mCRPC 患者中 pembro+enza 的治疗结果呈正相关。本研究这一探索性分析的样本量很小,观察到的结果需要综合考虑,谨慎解读。
表1:
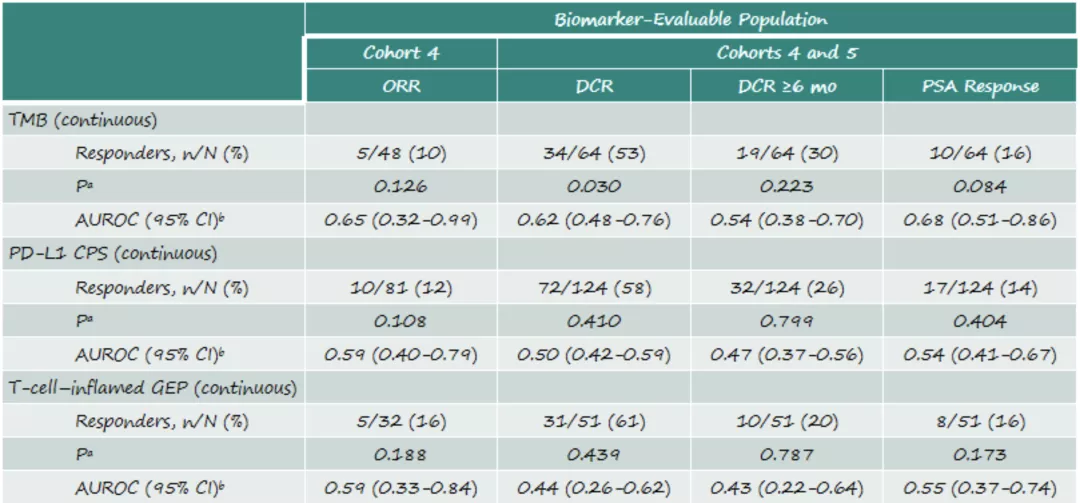
上述是KEYNOTE-365 队列A和KEYNOTE-199 队列4-5的最新研究进展,丰富了mCRPC的免疫治疗成果。目前免疫联合是mCRPC领域研发的重点方向,关于Pembro联合奥拉帕利、恩扎卢胺或多西他赛的III期研究正在开展中(KEYLYNK-010, NCT03834519; KEYNOTE-641, NCT03834493; KEYNOTE-921, NCT03834506)。
参考文献
[1] E. Yu. et al. Annals of Oncology (2021) 32 (suppl_5): S626-S677.
[2] E. Yu , et al. Annals of Oncology (2021) 32 (suppl_5): S382-S406.
[3] J.N. Graff. . et al. Annals of Oncology (2021) 32 (suppl_5): S382-S406.
免责声明:
本资讯由默沙东医学团队编辑提供,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
查看更多