查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





晚期肾透明细胞癌(ccRCC)治疗中,TKI耐药后选择匮乏、传统双免疫疗法毒性难控是临床痛点。中国原研的全球首个PD-1/CTLA-4双特异性抗体——艾托组合抗体,通过MabPair技术实现PD-1与CTLA-4 2:1协同抑制,Ⅰ期研究显示其单药≥3级免疫相关不良事件(irAE)发生率仅8.1%,联合方案一线治疗肾癌客观缓解率(ORR)达63.7%、疾病控制率(DCR)93.9%,凸显“强效低毒”优势。
本期特邀山东第一医科大学附属省立医院管勇医生分享一例右肾透明细胞癌术后合并多部位转移的患者,该患者初始接受培唑帕尼治疗因耐受差且症状进展停药,后采用艾托组合抗体联合阿昔替尼方案,治疗近3个月后转移灶显著缩小、减少,达到部分缓解(PR)的病例。同时特邀山东第一医科大学附属省立医院丁森泰教授对该病例进行深入点评,为晚期肾癌的临床诊疗提供新的思路和借鉴。
管勇 教授
山东省立医院副主任医师
硕士研究生导师
山东省医师协会干细胞与细胞转化医学委员会委员
山东省老年协会泌尿外科分会委员
山东省医学会男科学分会青年委员
山东省医师协会男科创新工程协会委员
病史
患者,男,50岁,因“腹腔镜下右肾根治性切除术后转移”就诊。
现病史:2023年11月2日因查体发现右肾肿瘤行右肾根治性切除术(RN),术后病理提示透明细胞癌3-4级,肿瘤直径5cm。术后定期复查,2025年3月25日CT检查发现术后转移。
查体:右侧肾区叩痛。浅表淋巴结未触及肿大,心、肺、腹部检查未见异常(-) ECOG评分:0分
辅助检查
2025年3月29日CT:右侧膈肌脚、腰大肌处见软组织肿块(临近骨质破坏),考虑转移灶;双肺多发小结节,较前增多,考虑转移瘤;肝内多发异常强化灶,胰头区异常强化灶,考虑转移瘤。

图1 2025年3月29日CT检查
诊断
右侧肾透明细胞癌术后转移
治疗经过
初始治疗:培唑帕尼单药耐受差,肾区胀痛加重
培唑帕尼800mg po qd治疗,仅用药1周,患者因不良反应(腹泻、乏力)及原有症状(肾区胀痛)加重,治疗耐受性差,遂停用该方案。
后续治疗:艾托组合抗体联合TKI,快速达PR且耐受良好
2025年4月4日 调整治疗方案为阿昔替尼片5mg po bid + 艾托组合抗体400mg ivdrip Q3w。治疗期间患者无明显不良反应,整体耐受良好。
2025年6月27日 随访CT诊断意见:1. 近右侧膈肌脚、腰大肌处软组织肿块转移治疗后,较前缩小;2. 肝内及胰头区转移瘤治疗后,较前缩小;3. 双肺多发小结节,较前明显减少、缩小。根据RECIST 1.1标准,疗效评估为部分缓解(PR)。
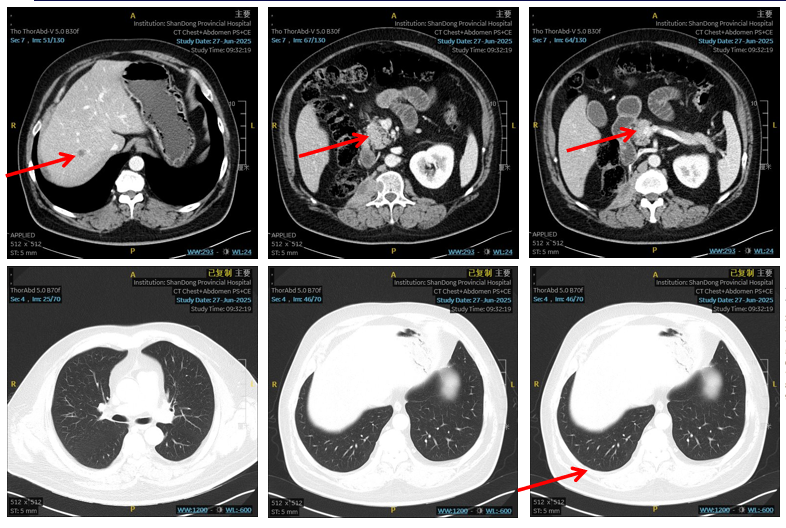
图2 2025年6月27日CT复查
丁森泰 教授
山东第一医科大学附属省立医院(山东省立医院)泌尿外科副主任医师、医学博士;
日本京都大学联合培养博士;美国西南医学中心高级访问学者;济南市高层次人才;
山东大学/山东第一医科大学 副教授、硕士研究生导师;
“一带一路”吉尔吉斯斯坦奥什国立大学 博士研究生导师
在泌尿系肿瘤的基础和临床治疗研究方面取得的研究成果在Journal of Urology、Cancer Research等SCI杂志发表文章二十余篇,发表中文核心期刊论著20余篇;
主持国家自然科学基金、山东省重点研发计划、山东省医药卫生科技发展计划和山东省自然科学、济南市科技发展计划等,参加国家及省市课题多项;
获得山东省药学会二等奖1项(第一位);山东省自然科学学术创新奖专家奖;山东省高等学校科学技术奖1项(第二位);医学会科技成果进步奖二等奖1项(第二位);
社会兼职:
山东省老年学与老年医学学会泌尿外科专业委员会 副主任委员;
中华医学会山东省泌尿外科学会 青年副主任委员;
中国医师协会男科医师分会 全国委员;
山东省医学伦理学学会泌尿肿瘤外科分会第一届理事会 副会长;
中国抗癌协会泌尿男生殖系肿瘤专业委员会 全国青年委员;
中国抗癌协会( CACA )第一届前列腺癌整合防筛专业委员会 全国委员
从“耐受失败”到“快速缓解”:艾托组合抗体联合TKI破解晚期肾癌治疗困境
对于晚期肾透明细胞癌患者,尤其是术后病理分级较高、合并多部位转移的患者,治疗方案的“有效性”与“耐受性”平衡直接决定预后。传统TKI单药治疗虽为经典选择,但部分患者因个体耐受性差异,易出现严重不良反应导致治疗中断。本例患者初始使用培唑帕尼仅1周,即因腹泻、乏力及肾区胀痛加重无法耐受,印证了TKI单药在部分高危患者中存在的局限性。
而艾托组合抗体联合阿昔替尼方案的应用,为这类患者提供了“高效且安全”的新选择。从机制来看,该方案实现了“免疫激活+抗血管生成”的协同增效:艾托组合抗体通过2:1固定比例的PD-1/CTLA-4双靶点抑制,一方面解除T细胞功能耗竭,另一方面减少肿瘤微环境中调节性T细胞(Treg)数量,双重激活抗肿瘤免疫应答;阿昔替尼则通过抑制VEGFR改善肿瘤血管异常,促进免疫细胞向肿瘤微环境浸润,进一步放大免疫治疗效果。
这种协同机制在本例中体现为“快速且深度的疗效”。从2025年4月4日启动治疗至6月27日评估,仅2个多月时间,患者右侧膈肌脚、腰大肌转移灶缩小,肝、胰头转移灶缩小,双肺转移结节明显减少、缩小,顺利达到PR,且全程无明显不良反应。
值得一提的是,在今年的ESMO大会中,艾托组合抗体联合小分子TKI仑伐替尼治疗未经治疗的透明细胞肾细胞癌患者安全性和有效性的1b期研究的结果即将公布,有望为协同增效理论提供更多临床证据。
技术革新赋能临床:艾托组合抗体的“低毒”优势源于机制突破
艾托组合抗体的“低毒”特性并非偶然,而是基于MabPair抗体工程技术的精准设计。与传统双免疫联合治疗不同,该药物通过基因工程将抗PD-1与抗CTLA-4抗体整合于同一分子,实现2:1固定比例协同,既避免了两种抗体单独给药时可能出现的剂量波动与毒性叠加,又通过优化CTLA-4抗体半衰期、调控Fc段功能,显著降低免疫相关不良反应风险。临床研究数据显示,其单药治疗晚期实体瘤的≥3级irAE发生率仅8.1%,而本例患者联合阿昔替尼后仍保持良好耐受性,进一步验证了该药物在联合治疗场景下的安全性优势。
对于合并多部位转移的晚期肾癌患者,长期耐受治疗是实现持续获益的前提。本例患者ECOG评分为0分,身体基础状态较好,但初始TKI单药即出现明显不适;而换用艾托组合抗体联合方案后,无不良反应困扰,既能保证治疗依从性,也为后续长期治疗、维持疗效奠定基础。这提示,在晚期肾癌治疗中,选择“患者可耐受的高效方案”,比单纯追求“理论疗效”更具临床意义。
中国原研的临床价值:为晚期肾癌治疗提供“本土化”解决方案
艾托组合抗体作为全球首个基于MabPair技术的PD-1/CTLA-4双特异性抗体,其研发与临床应用凸显了中国原研药物在肿瘤治疗领域的创新实力。从临床数据来看,该药物在晚期肾癌患者中展现出优异的抗肿瘤活性:此前研究显示,其单药治疗晚期肾癌的ORR达27.8%、DCR达72.2%,均高于其他实体瘤人群;而联合VEGFR-TKI后,更能进一步提升疗效,如本例快速达PR的表现,与联合方案“协同增效”的机制预期高度一致。
此外,中国原研药物在“患者适配性”上更具优势——其临床研究多纳入中国患者,疗效与安全性数据更贴合中国晚期肾癌患者的群体特征,为临床诊疗提供更精准的参考。本例患者作为中国原研药物联合方案的获益者,从治疗不耐受到快速缓解的诊疗历程,不仅验证了该方案的临床价值,也为更多类似晚期肾癌患者的治疗提供了可借鉴的实践范本。
未来,随着对艾托组合抗体联合方案生物标志物的深入探索、长期随访数据的积累,以及与其他治疗手段联合策略的优化,有望为晚期肾癌患者带来更长期的生存获益,推动中国原研方案在全球晚期肾癌治疗领域发挥更大作用。
本文由管勇教授、丁森泰教授审校
查看更多