查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2023年10月20-24日,全球肿瘤学盛会——欧洲肿瘤内科学会(ESMO)年会在西班牙马德里成功举办。尽管神经内分泌肿瘤属于罕见肿瘤,但其治疗手段丰富多样,包括手术、放射介入治疗、放疗、肽受体介导的放射性核素治疗(PRRT)以及系统治疗如分子靶向治疗、SSA治疗和化疗等。如何在众多治疗方案中做出最佳选择,是临床医生亟待解决的问题。在ESMO年会上,神经内分泌肿瘤领域的报道精彩纷呈,涵盖了基础、转化和临床研究等多个方面。我们邀请华西医院曹丹教授及其团队精选了其中三项研究与读者分享。
靶向治疗的新星——
卡博替尼CABINET研究结果令人振奋
本次ESMO大会上神经内分泌肿瘤领域最耀眼的明星当属卡博替尼。卡博替尼是一种多靶点的小分子酪氨酸激酶抑制剂,其靶点多达9个(MET、VEGFR1、VEGFR2、VEGFR3、ROS1、RET、AXL、NTRK、KIT),目前已被美国FDA批准用于甲状腺髓样癌、肾癌和肝癌,在多种实体瘤中均有突出的疗效。来自美国Dana-Farber癌症研究所的Jennifer Chan博士报道了卡博替尼治疗晚期神经内分泌肿瘤的III期临床研究[1](CABINET研究)的阳性结果。该研究的主要目的为评估卡博替尼对比安慰剂在晚期中高分化神经内分泌肿瘤后线治疗的疗效,所有受试者需满足分级为G1-3,原发灶不论,除了长效生长抑素类似物(SSA)以外的至少一线标准治疗后进展(包括依维莫司、舒尼替尼、Lu-177核素治疗、化疗等);研究按照原发灶部位分为胰腺神经内分泌瘤(pNET)和胰腺外神经内分泌瘤(epNET)两个队列,按照2:1随机分配至卡博替尼60mg每日一次口服组或安慰剂组,直至疾病进展,揭盲后安慰剂组可交叉到卡博替尼组,研究过程中允许同时使用SSA,主要研究终点为PFS,次要研究终点为OS、ORR、安全性及耐受性。
图1.CABINET研究设计
由于中期分析疗效较好,该研究团队决定提前终止入组。截至2023年6月,epNET队列共入组197例,原发灶主要来源于胃肠道(>50%),pNET队列共入组93例,两个队列均达到主要研究终点:卡博替尼组中位PFS显著优于安慰剂组(epNET队列:8.3 vs. 3.2个月,HR=0.45,P<0.0001;pNET队列:11.4 vs. 3.0个月,HR=0.27,P<0.0001)。与安慰剂组相比,卡博替尼组的ORR也有明显改善(epNET队列:4% vs. 1%;pNET队列:18% vs. 6%),但大会报道并未公布统计学P值。在中位OS方面,由于疾病进展揭盲后安慰剂组可交叉至卡博替尼组,因此两组的OS并无显著性差异(epNET队列:21.9 vs. 22.4个月,HR=0.9,P=0.34;pNET队列:43.5 vs. 31.0个月,HR=0.77,P=0.26)。卡博替尼组主要不良反应为高血压、乏力、腹泻、高血糖、血栓栓塞、手足综合征,但总体毒副反应可耐受。
图2.epNET及pNET队列的PFS
图3.epNET及pNET队列的ORR
图4.epNET及pNET队列的OS
专家点评:虽然晚期神经内分泌瘤预后相对较好,但标准治疗失败后的患者系统治疗的选择非常有限,疗效欠佳。CABINET研究入组的受试者均为除SSA外至少一种标准治疗失败的患者:在pNET队列中,高达82%的受试者使用过依维莫司,52%的受试者使用过Lu-177核素治疗,29%使用过舒尼替尼,68%使用过替莫唑胺为主的化疗,因此大部分受试者既往治疗线数较多,几乎无标准治疗药物可用。卡博替尼无疑为经治神经内分泌瘤患者提供了一种全新的选择,尤其在分化良好的胰腺神经内分泌瘤中疗效显著,中位PFS长达11.4个月,有望成为后线治疗的标准推荐。
同时我们看到索凡替尼在SANET-p研究[2]和SANET-ep[3]研究中,PFS分别为10.9个月和9.2个月,ORR分别为19.2%和10.3%。目前索凡替尼也是全球唯一覆盖所有部位来源NET的治疗药物,无论Ki67指数、肿瘤负荷、肿瘤进展速度以及SSTR表达状态,索凡替尼在PFS、ORR、肿瘤退缩率均有显著获益。CSCO、CACA、CMA等各大指南/共识均推荐索凡替尼作为神经内分泌肿瘤的一线标准治疗。
因人而异,精准施治——
基于MGMT状态优选化疗药物
分化良好的神经内分泌瘤有效的化疗药物不多,主要为烷化剂(如替莫唑胺、链脲霉素、达卡巴嗪)或奥沙利铂为基础的化疗。O6甲基鸟嘌呤DNA甲基转移酶(MGMT)参与烷化剂所致DNA损伤修复过程,有回顾性研究提示MGMT基因启动子区甲基化或免疫组化MGMT蛋白表达缺失为烷化剂的疗效预测因子,但仍有争议。来自法国里昂医院的Thomas Walter教授团队开展了一项多中心、随机、对照、II期研究[4](MGMT-NET研究),旨在基于MGMT状态探索神经内分泌瘤的优选化疗药物。MGMT缺失(dMGMT)定义为MGMT基因启动子区甲基化或MGMT蛋白免疫组化表达缺失,反之则为MGMT完整(pMGMT)。该研究主要入组标准为:晚期神经内分泌瘤,原发灶位于胰腺、胸部或者不明;拟采用系统化疗;有足够的组织标本可用于MGMT分析。dMGMT的受试者按照2:1随机分配到烷化剂为主的化疗组(CAPTEM或氟尿嘧啶联合链脲霉素或氟尿嘧啶联合达卡巴嗪)或奥沙利铂为主的化疗组(GEMOX或FOLFOX或CAPOX),pMGMT组按照1:1随机分配到两种化疗方案组。主要研究终点为3个月ORR率(预计dMGMT组比pMGMT组使用烷化剂的3个月ORR率提高35%);次要研究终点为ORR、PFS、OS及安全性。
图1.MGMT-NET研究设计
该研究共入组102例符合受试者,平均随访29.3个月,其中dMGMT组58例,pMGMT组52例,绝大部分受试者为G1(28%)或G2(60%),原发灶主要来源于胰腺(54%)和肺(37%),中位Ki67指数为10%左右,烷化剂为主的化疗方案主要为CAPTEM(50%)和氟尿嘧啶联合达卡巴嗪(45.2%),奥沙利铂为主的化疗方案主要为GEMOX(81.4%)和FOLFOX(14%)。结果表明,dMGMT组比pMGMT组使用烷化剂的疗效较好,但3个月ORR率并未达到预设终点(提高35%),分别为31%和12%。在dMGMT组,烷化剂为主的方案比奥沙利铂为主的方案疗效更佳(ORR:56% vs. 21%),而在pMGMT组,奥沙利铂为主的方案比烷化剂缓解率更高(ORR:39% vs. 18%),表1展示了主要的疗效数据。
表1.pMGMT及dMGMT两组患者采用不同方案的疗效
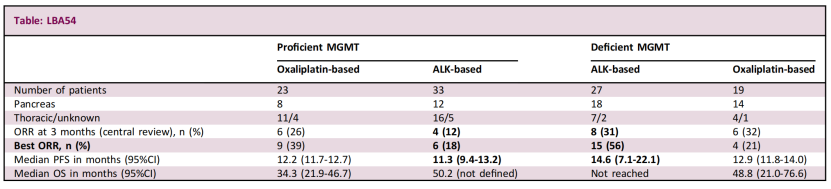
图2.烷化剂为主的方案的疗效与MGMT状态有关
专家点评:对于Ki67指数较高的G2-3神经内分泌瘤患者,烷化剂为主的化疗是常用的治疗方案之一,但其疗效与MGMT的状态是否有关联,目前尚未有确切结论。MGMT-NET研究虽然并未达到主要终点,但其ORR、PFS等结果表明,MGMT缺失的患者采用烷化剂治疗效果较好,而MGMT完整的患者采用奥沙利铂为主的方案效果更佳。但该研究样本量较小,且MGMT甲基化和免疫组化表达缺失的具体判读标准尚有待深入研究,期待大样本随机对照临床试验进一步确定MGMT的状态对化疗疗效的影响。
直肠NET的区域淋巴结转移的预测模型
近年来,随着内镜检查等早期检测手段的不断进步,直肠NET的检出率逐渐提高,虽然大多数患者属于早期、分化良好,但仍有10%左右会发生区域淋巴结转移甚至远处转移。早期患者行内镜下切除即可根治,而合并淋巴结转移的患者需要外科手术清扫淋巴结,术后随访复查的频率也会相应提高。如何预测直肠NET的区域淋巴结转移的风险成了诊疗的重点和难点。四川大学华西医院腹部肿瘤科曹丹教授团队利用美国SEER数据库1243例直肠NET患者作为训练集,建立了预测直肠NET发生区域淋巴结转移的风险模型[5](包含肿瘤大小、T分期、分级、年龄四个因素),该模型的内部验证一致性指数(C-index)高达0.968,利用华西医院数据库进行外部验证的C-index达到0.877,预测准确性较高。具体而言,肿瘤直径≥20mm,T2及以上,分级G2及以上,年龄≥53岁为区域淋巴结转移的高危因素。
专家点评:利用该风险模型,我们可以预测直肠NET患者发生区域淋巴结转移的风险,实现更加精准的分层分级,对于高风险患者可避免漏诊风险,并早期发现转移灶积极干预仍可追求根治,而对于低风险患者可避免不必要的检查和治疗,将精准医学的理念更好地应用于临床实践。
曹丹 教授
主任医师,博士生导师
四川大学华西医院腹部肿瘤科主任
四川省卫健委学术技术带头人
中国抗癌协会神经内分泌肿瘤专委会常委
中国抗癌协会整合肿瘤肾脏病学专委会常委
中国抗癌协会胰腺癌专委会委员
CSCO胰腺癌/CSCO神经内分泌肿瘤专委会委员
中国医促会神经内分泌肿瘤分会委员
四川省肿瘤学会神经内分泌肿瘤专委会主任委员
四川省医促会肿瘤分子靶向治疗专委会候任主任委员
四川省抗癌协会肿瘤内分泌专委会候任主任委员
国家自然科学基金通信评审专家
《Frontiers in Pharmacology 》SCI杂志编委
以第一作者或通讯作者发表SCI论文40余篇
主持多项国家自然科学基金、省科技厅基金、华西医院1.3.5重大项目
李晓芬 教授
肿瘤学博士,四川大学华西医院腹部肿瘤科主治医师
四川省抗癌协会肿瘤内分泌专委会委员兼秘书
四川省抗癌协会肿瘤支持治疗与全程管理专委会委员
四川省肿瘤学会神经内分泌肿瘤专委会委员兼秘书
四川省预防医学会基层肿瘤防治专委会委员
四川省国际医学交流促进会消化道肿瘤专委会委员
四川省国际医学交流促进会肿瘤分子靶向治疗专委会委员
成都市抗癌协会消化道肿瘤MDT专委会委员
以第一作者或共同第一作者身份发表文章20余篇,其中被SCI收录10余篇
负责四川省科技厅及卫健委项目2项,参与多项国家级课题
参考文献:
[1] 2023 ESMO. LBA53.
[2] Xu J, et al. Lancet Oncol. 2020 Nov;21(11):1489-1499.
[3] Zhou Z, et al. 2020 ESMO Abstract 4261.
[4] 2023 ESMO. LBA54.
[5] 2023 ESMO. 1196P.
本资料仅代表个人观点,旨在促进学术信息的沟通和交流。本资料仅供医疗卫生专业人士作学术参考,而非针对一般公众,亦非广告宣传。处方请参考国家药品监督管理局批准的药品说明书。请勿分发或转发本资料。
本资料由和黄医药提供支持。
NP-STD-23N1498-Valid Until-2025-October
查看更多