查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





面对晚期结直肠癌多发转移,呋喹替尼如何提供治疗方案?
对于结直肠癌(CRC)的治疗,早期手术切除仍是现在唯一可能达到治愈水平的治疗手段,但约25%患者在初诊时已发生转移[1],基本丧失手术的机会。随着分子靶向药物的进展和应用,晚期CRC患者的生存期得到了显著改善[2]。据统计,在2003年至2015年期间,中国CRC患者5年生存率提高接近10%[3]。
呋喹替尼作为我国自主研发治疗转移性结直肠癌(mCRC)的新型小分子靶向药物,2018年获得国家药品监督管理局(NMPA)批准并正式上市。上市5年来,接受过呋喹替尼治疗的晚期结直肠癌患者已超过7万名,为相关患者带来了一定的生存获益。下面分享一例CRC多发肝转移患者后线应用呋喹替尼有效管理的案例,期待为临床用药带来新思考。
(以下病例仅系相关主治医生在执业过程中的病情回顾与评述,个体病例通常具有差异性,具体治疗方案及用药应当结合个体情况并严格遵循医嘱。)
患者男,69岁;身高:165cm,体重:63kg,体表面积:1.66m2;ECOG评分:0分。
主诉:大便带血2月。
现病史:2021年4月23日我院肠镜见:距肛缘5cm直肠菜花样包块,占3/4周径,表面溃烂有黄苔,质地脆,易出血,病理诊断:直肠腺癌。
既往史:高血压病20+年,2型糖尿病5+年,腔隙性脑梗1+年;
个人史:吸烟20余年,10支/天;饮酒30年,平均100ml/天;家族史无特殊。
体格检查:腹部无明显阳性体征,肛门指检(膝胸位):距肛缘5cm直肠扪及菜花样包块,占3/4周径,退出指套有血迹。
胸腹部增强CT(2021年04月26日):1.直肠中下段不规则增厚、强化,考虑直肠癌可能;2.肝后叶占位性病变考虑转移性肿瘤(范围约4.2×2.9cm)。
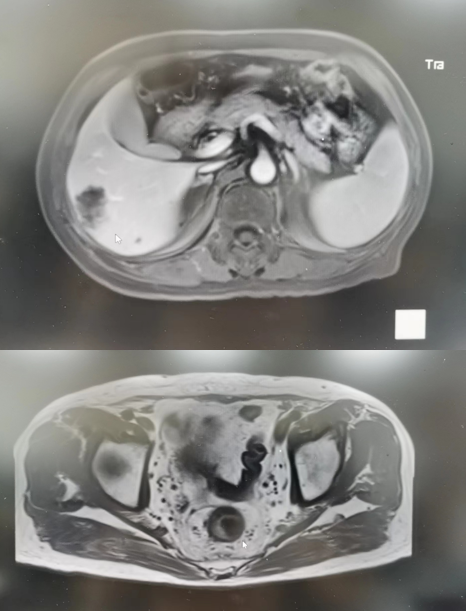
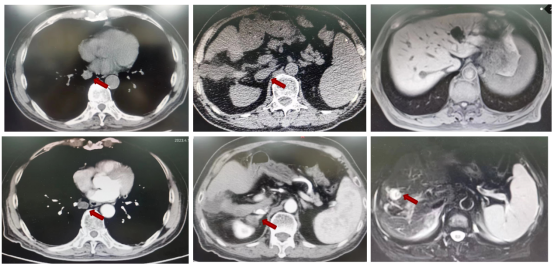
盆腔MRI(2021年04月26日):1.直肠管壁及周围改变,考虑中位直肠癌:T4aN2,CRM(阳性),EMVI(阳性)(图1)。
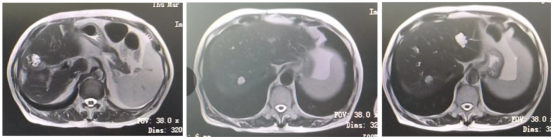
腹部MRI(2021年05月05日):1.肝右后叶下段(VI段)占位性病变,考虑转移(5×3.7cm)(图2)。
肿瘤标志物(2021年04月28日):癌胚抗原(CEA) 27.21ng/ml、糖类抗原199(CA199)>800U/ml、糖类抗原242(CA242)>500U/ml
基因检测:KRAS、NRAS、BRAF无突变,pMMR。

图1 2021年04月26日盆腔MRI

图2 2021年05月05日上腹部MRI
1.中位直肠腺癌(cT4aN2M1a,IVA期,KRAS、NRAS、BRAF野生型,pMMR)
2.肝转移癌(CRS评分:3分)
3.高血压病3级
4.2型糖尿病
胃肠肿瘤MDT讨论认为患者的原发病灶及转移灶是可切除状态,但生物学行为较差,经医患沟通后,决定先行西妥昔单抗+mFOLFOX6方案转化治疗再复查评估,外科手术治疗后再继续围手术期治疗。患者于2021年5月6日至2021年7月2日接受西妥昔单抗+mFOLFOX6治疗5周期;期间复查腹部及盆腔MRI,提示肝右后叶占位较前缩小(图3上),直肠管壁及周围改变较前缩小(图3下)。疗效评价:部分缓解(PR)。
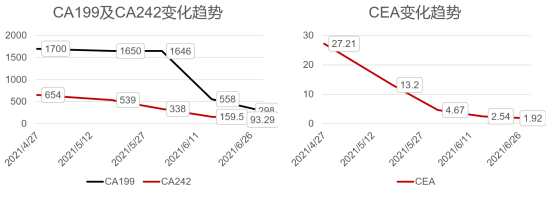
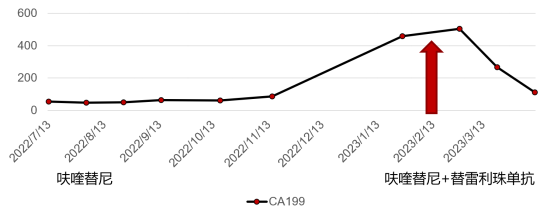
该阶段治疗过程中,患者肿瘤标志物CEA、CA199、CA242均逐渐下降(图4):


2021年8月23日,患者在排除手术禁忌后行腹腔镜直肠全系膜切除术、乙状结肠腹壁造口术。术后病理示:黏液腺癌,癌组织侵及浆膜下;神经侵犯(+)、脉管内癌栓(+)近肿瘤切缘、远肿瘤切缘、环周切缘未见癌组织;肠周淋巴结(2/12)查见癌转移,另见癌结节5枚;病理分期:pT3N1cM1.Ki-67 90%。错配修复蛋白MSH6、MLH1、MSH2、PMS2均阳性表达,错配修复功能正常(pMMR);TRG评分=2分
2021年09月16日,行经腹腔镜中转右肝部分切除术,术后病理示:黏液腺癌,结合免疫组化及病史符合肠来源腺癌,癌组织紧邻肝脏被膜,可见脉管内癌栓,未见明确神经侵犯,周围肝示慢性炎,轻度脂肪样变性,肝切缘未见明确癌组织。Ki-67 60%。
2021年10月8日至2022年1月13日,患者接受西妥昔单抗+mFOLFOX6治疗5周期。
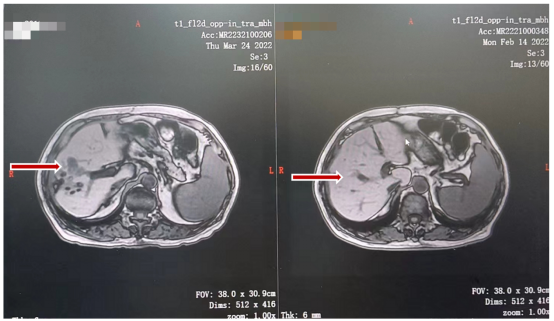
2022年2月复查腹部MRI提示肝脏Ⅳ段出现新增病灶,2022年02月24日行第一次超声引导下经肝肿瘤射频消融术(图5)。
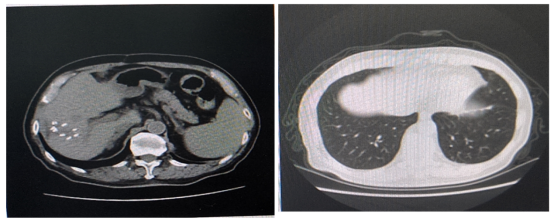
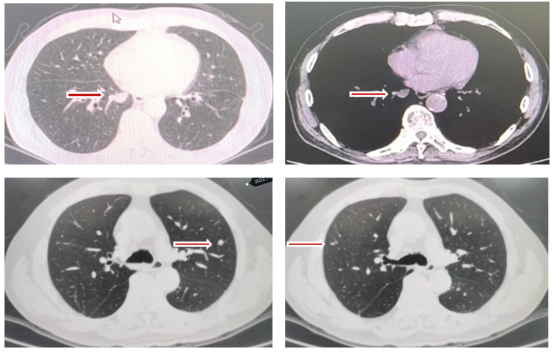
2022年2月复查胸部CT提示左肺上叶尖后段出现微小结节,最大直径0.3cm,建议治疗中密切随访(图6)。

患者于2022年3月31日至2022年5月12日行二线贝伐珠单抗+XELIRI治疗3周期。
2022年6月8日,肝Ⅴ、Ⅶ段出现新增病灶,行第二次超声引导下经肝肿瘤射频消融术,术后1月复查,肝脏病灶未见明显变化(图7)。

因化疗耐受性较差,患者于2022年6月23日至2022年8月25日行贝伐珠单抗+卡培他滨治疗3周期。期间出现中度骨髓抑制,2022年7月23日血小板降至48*10^9/L。2022年7月复查胸部CT,提示双肺结节增大、增多(图8)。疗效评价:疾病进展(PD)。

2022年8月,患者病情进展、骨髓抑制、自身无法耐受贝伐珠单抗+卡培他滨(PS评分:1分;升血小板治疗后血小板升至60-80*10^9/L),开启三线呋喹替尼单药治疗。
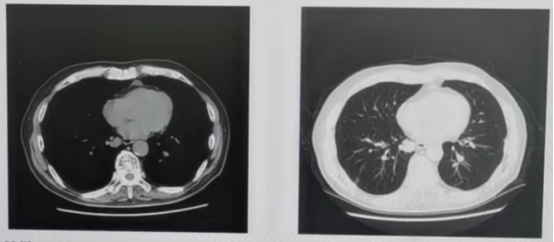
2023年1月复查胸部CT检查,提示双肺多个结节较前(2022年7月)增大,右侧肾上腺结节(图9)。疗效评价:PD。

2023年2月至今接受呋喹替尼联合替雷利珠单抗治疗。2023年4月复查:疾病稳定(SD)。

2023年1月、4月复查胸部CT:肺部病灶部分缩小;上腹部MRI:肝V、VII段异常信号影(较大者大小2.5*1.6cm),较前变化不大,右侧肾上腺转移病灶增大(图11)。

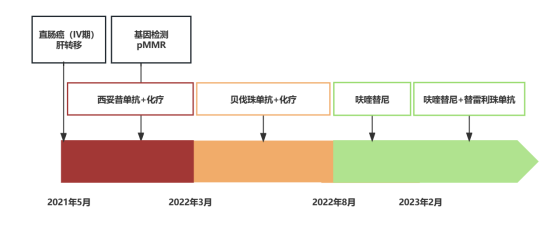
该病例为一名老年男性,因发现大便带血2月入院,入院诊断为:中位直肠腺癌(cT4aN2M1a,IVA期,KRAS、NRAS、BRAF野生型,pMMR);肝转移癌(CRS评分:3分)。经西妥昔单抗+mFOLFOX6方案转化治疗后先行腹腔镜直肠全系膜切除术、乙状结肠腹壁造口术,术后诊断为:(pT3N1cM1a,pMMR);再行经腹腔镜中转右肝部分切除术,术后证实为肝转移癌。患者一线接受西妥昔单抗+mFOLFOX6方案治疗,后出现肝脏、肺部新增转移病灶,行第一次超声引导下经肝肿瘤射频消融术,并接受二线贝伐珠单抗+XELIRI治疗,后出现肝脏新增病灶,行第二次超声引导下经肝肿瘤射频消融术及贝伐珠单抗+卡培他滨方案治疗,期间出现病情进展、骨髓抑制、自身无法耐受等情况,三线接受呋喹替尼单药治疗,进展后序贯呋喹替尼联合替雷利珠单抗方案治疗,截至病例征集时间,疗效评价持续SD(图12)。

高选择性小分子酪氨酸激酶抑制剂(TKI)呋喹替尼作用于血管内皮生长因子受体(VEGFR)-1/2/3,抑制血管生成,从而抑制肿瘤生长。登顶《JAMA》杂志的FRESCO研究[4]证明呋喹替尼单药在晚期肠癌治疗中表现出良好的疗效与安全性。而在李进教授团队领衔开展的呋喹替尼联合信迪利单抗方案[5]研究显示,呋喹替尼联合免疫治疗使MSS/pMMR mCRC患者的中位无进展生存期(mPFS)和中位总生存期(mOS)分别延长至6.9个月和20.0个月,客观缓解率(ORR)达20.0%,疾病控制率(DCR)达100%,提示呋喹替尼联合免疫治疗在MSS/pMMR mCRC具有一定的治疗前景。
而我们在临床实践中发现,呋喹替尼单药序贯联合免疫作为一种有益的治疗方案的组合,或可进一步提升mCRC患者的生存获益,这一想法也得到了许多中心真实世界研究的探索的验证。2022年欧洲肿瘤内科学会(ESMO)年会上发布了辽宁省肿瘤医院PD-1抑制剂联合TKI在对TKI高应答的MSS/pMMR型mCRC患者中的疗效与安全性的结果[6]。结果显示,呋喹替尼组有更多患者进入高应答组(序贯组)(11/15),序贯组mPFS为13.2个月(95%CI,8.3-18.1),9个月的PFS率为72.6%,mOS未达到。在不良反应方面,序贯组3-4级不良反应主要为高血压、蛋白尿、手足皮肤反应等,其在有效处理后均能得到明显缓解,表明呋喹替尼单药序贯联合免疫治疗方案的疗效与安全性良好。
无独有偶,2022年ESMO胃肠肿瘤大会(ESMO GI)上发布的河南省肿瘤医院开展的呋喹替尼治疗mCRC的真实世界研究数据[7]入组了71例mCRC患者,分为呋喹替尼单药组、联合免疫治疗组和单药序贯联合免疫治疗组,总体人群的mPFS为6.4个月,其中呋喹替尼单药组的mPFS为5.3个月;单药序贯联合免疫治疗组取得了最长12.8个月的mPFS,为mCRC治疗带来新思路。
在本病例中,三线接受呋喹替尼单药治疗,进展后序贯联合免疫治疗为MSS/pMMR mCRC患者带来持续的SD,安全性耐受性良好,是呋喹替尼在真实世界中为mCRC患者带来生存获益的又一力证。期待未来通过以呋喹替尼为基础的更多治疗方案的组合尝试,为肿瘤患者带来延长生存的助益。


查看更多