查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





本文专家 树兰(杭州)医院 郑赟
导读
近年来,随着对肿瘤微环境认识的不断深入,免疫治疗代表性药物——免疫检查点抑制剂(ICIs)成了肿瘤治疗领域的研究热点。在多个癌种的治疗中,ICIs治疗显示出明显的生存优势 ,但也有多项研究报道,个别患者在使用免疫检查点抑制剂后病情非但未见好转,还出现了短期内肿瘤的快速增长,且预后较差,这种现象被称为“超进展”(HPD)。
如何评估HPD的发生?HPD的潜在预测因素包括哪些?本文将带你全面认识免疫治疗超进展。
Part1
先来回顾一下免疫治疗的“Bright Side”
免疫治疗在抗肿瘤领域逐渐占据重要地位,方兴未艾。目前,获得监管批准最多的免疫治疗药物是以PD-1/PD-L1单抗为代表的ICIs,涉及肺癌、消化道肿瘤等十余个癌种。
截至2021年9月15日,FDA批准了71项ICIs治疗适应证,而国内NMPA也批准了11个免疫检查点抑制剂共计39项适应证,近一半为一线治疗适应证,具体获批情况见下图:
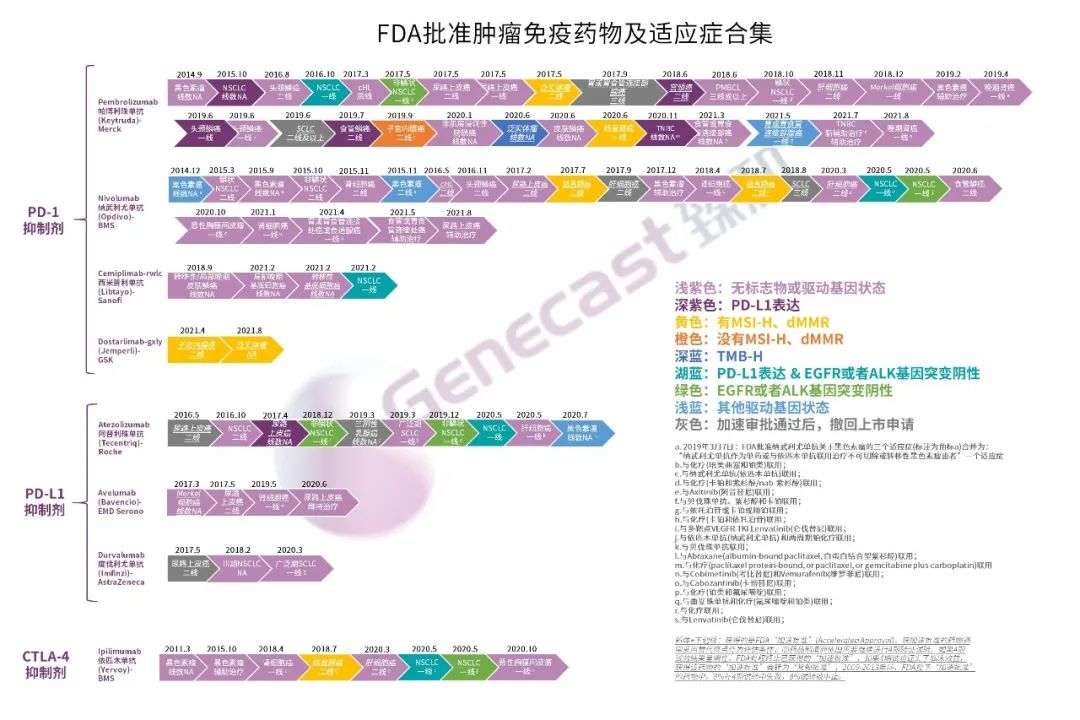
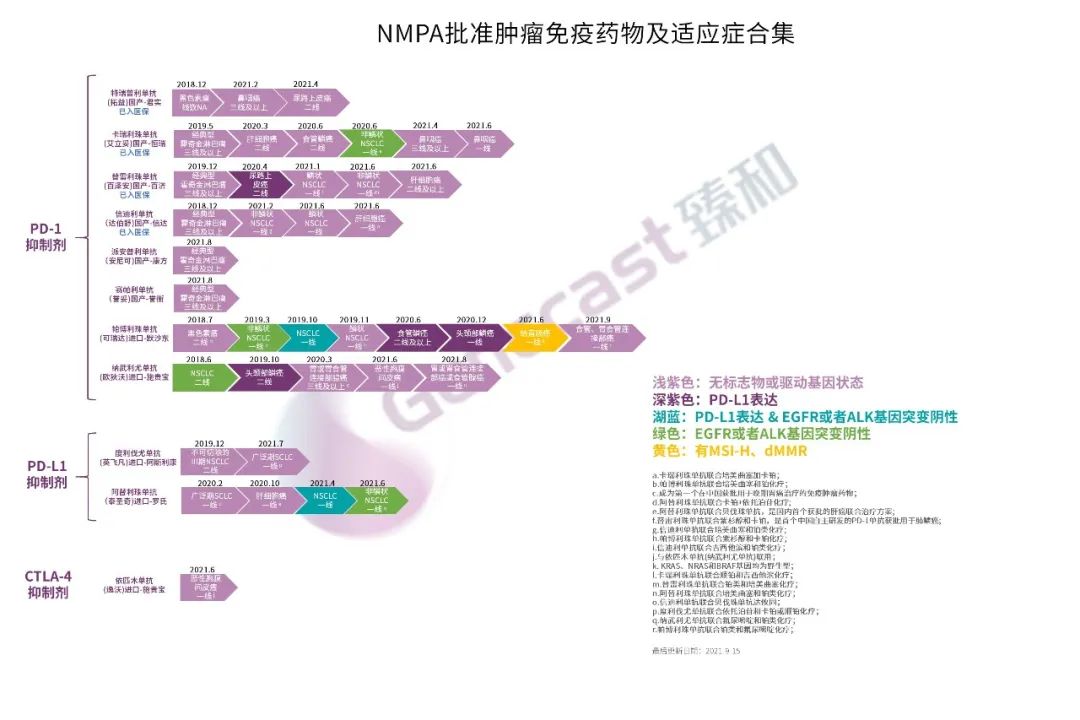
有光明的地方通常也伴随阴影,在免疫治疗高歌勇进的同时,它的Dark Side也逐渐显现,并且不得不引起关注。
Part2
揭秘免疫治疗Dark Side——超进展
2.1超进展(HPD)的评估要素
首次报道
2016年,Chubachi团队首次报道了1例接受ICIs治疗后出现疾病快速进展的NSCLC病例,患者使用PD-1抑制剂6周后,肿瘤快速增长并出现肺转移和脑转移灶。癌胚抗原在PD-1抑制剂治疗开始后的8周内从360.4ng/ml升至1316.0 ng/ml。
首次定义
2017年,Champiat团队首次提出免疫治疗相关超进展的定义,即患者接受PD-1/PD-L1抑制剂治疗前后对比,肿瘤生长速率(tumor growth rate,TGR)增加≥2倍的疾病进展现象。
此后,不断有学者对HPD的定义进行完善和补充。但目前为止,国际上仍无HPD的统一定义。
#HPD的评估要素#
分析不同文献中的HPD定义可以发现,HPD常见的评估要素主要包括以下三个方面:肿瘤增长速度的计算、是否考虑新出现的病灶和治疗失败时间(TTF)。
其中对于肿瘤增长速度的计算可以大致分为以下四大类:
(1)肿瘤生长速率(TGR)比值,比较治疗前后肿瘤体积增加的速度;
*TGR定义为在1个月内肿瘤体积增加的百分比,TGR的评估是基于RECIST 1.1标准,治疗前后靶病灶最大直径之和的变化,并使用自然对数进行校正。
(2)肿瘤生长动力学(TGK)比值,比较治疗前后肿瘤大小增加的速度;
*TGK定义为单位时间内肿瘤大小的变化(毫米/天),TGK的评估与TGR相似,也测量靶病灶最大直径之和的变化,但未使用对数校正。
(3)早期肿瘤负荷,比较基线和治疗后第一个时间点之间早期肿瘤负荷增加的速度;
(4)由以上几个分类组成的复合概念。
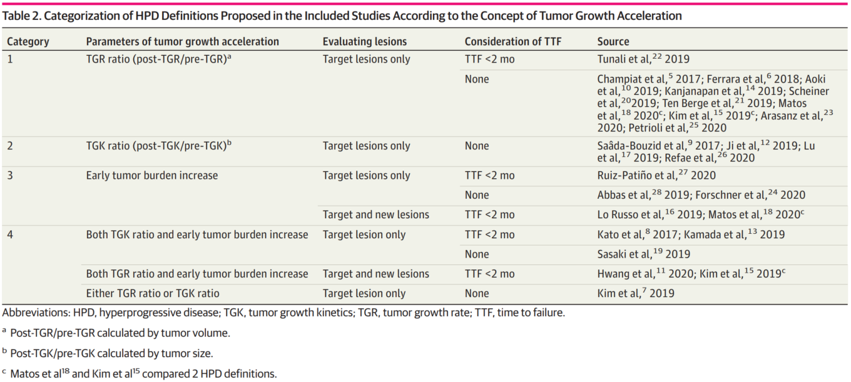
TGR和TGK的计算依赖于免疫治疗前后的影像学评估结果,临床中,较少患者能提供完整的免疫治疗前以及基线时间点的影像学资料,导致TGR或者TGK无法计算或者计算结果不准确。
2.2HPD的发生率和预后
由于HPD的定义标准和样本量不同,HPD的发生率在不同癌种和不同研究类型中存在较大差异。PD-1/PD-L1抑制剂相关的HPD发生率在5.9%-43.1%不等,合并发病率为13.4%(95%CI:10.2-16.6),CTLA-4抑制剂单药治疗未见HPD报道。
HPD患者预后更差,中位总生存(OS)期3.4个月,与非HPD患者的6.2个月相比,差异有统计学意义(P=0.003)。
总体来看,HPD的发生率不容小觑,HPD的发生也通常预示着更差的预后。那么HPD是免疫单药治疗的独有现象吗?ICIs与化疗的联合用药方案HPD发生率如何呢?
超进展(HPD)并不是免疫治疗的独有反应模式,在靶向治疗和化疗中也有报道,但发生率不及免疫治疗高。
有研究探讨了免疫联合化疗方案的HPD发生率,发现接受联合治疗的患者HPD发生率明显低于PD-1/PD-L1抑制剂单药治疗的患者(免疫联合化疗组:1/34,2.9%;免疫单药组:25/142,17.6%;p=0.031)。研究结果表明,ICIs联合化疗有降低HPD发生率的可能性,但需要大样本前瞻性研究进一步验证。
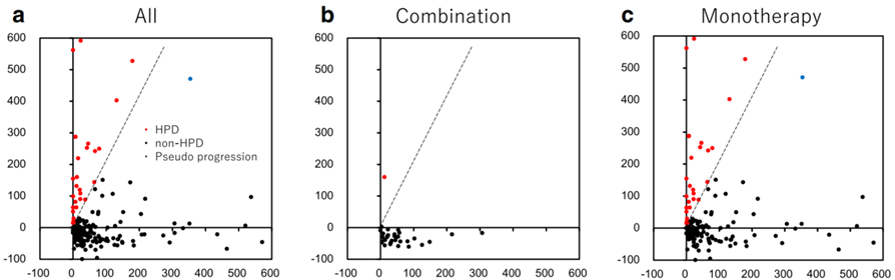
2.3HPD发生的机制
关于免疫检查点抑制剂导致超进展发生的机制仍不清楚,多位学者提出的研究假说认为PD-1通路的阻断可能引发复杂的级联反应,通过介导免疫抑制或直接加速肿瘤生长等机制,使得肿瘤的免疫微环境发生了变化,促使超进展的发生。
研究显示:PD-1抑制剂治疗后,可诱导Treg细胞的活化和扩增,引发免疫抑制。由于PD-1的缺失,耗竭CD8+T细胞的大量增殖和分化,同时其他免疫检查点分子(如 CTLA-4、LAG3等)出现代偿性表达上调,最终降低免疫杀伤能力,导致肿瘤的加速生长。
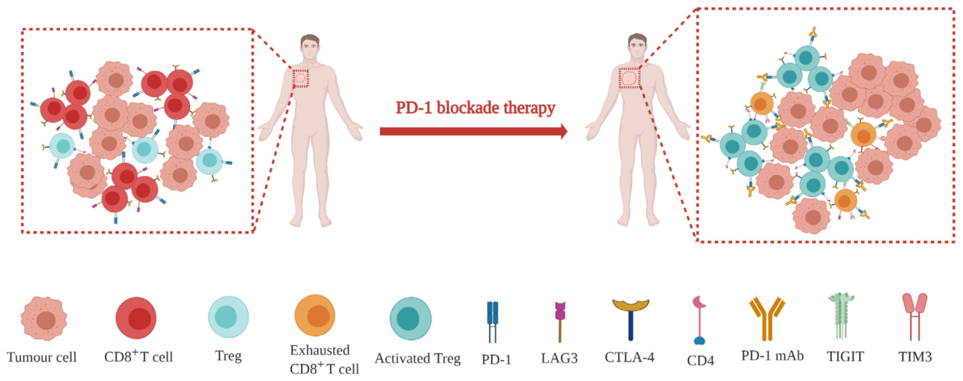
此外,致癌信号的激活和促肿瘤细胞因子的调节也可能是HPD发生的潜在机制。
对于HPD发生机制的探索主要还停留在假说和小样本验证试验。未来,期待更多针对HPD肿瘤免疫微环境的大样本探索研究。
2.4HPD的预测因素
ICIs治疗相关的超进展通常预示较差的临床预后,因此非常有必要去探索HPD的预测因素,以便于及早做出治疗决策不贻误病情。
(1)临床特征
研究显示:ICIs治疗相关的HPD与年龄(大于65岁)、性别(女性)、肿瘤复发(局部复发)、转移灶数目(2个以上转移灶)和体能评分PS(PS评分低)等因素有关。
(2)潜在生物标志物

Part3
同样是短期内肿瘤快速增长,“真”、“假”进展有何不同?
3.1假性进展(Pseudoprogression)是什么?
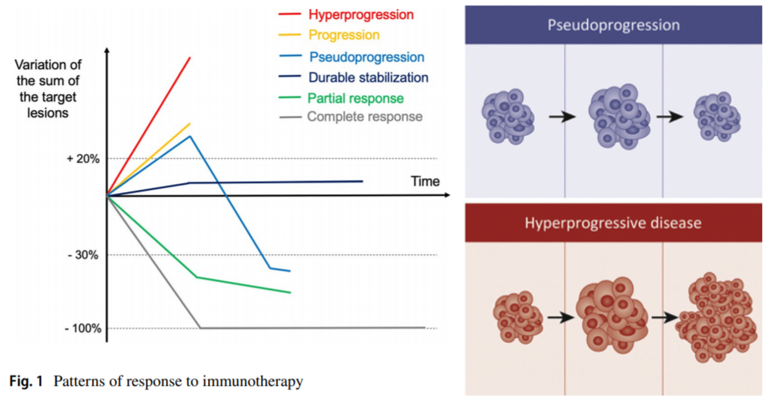
与超进展非常容易混淆的是另外一种免疫治疗反应模式:假性进展。研究显示,接受ICIs治疗的患者假性进展率不超过10%。
假性进展主要由于大量免疫细胞进入肿瘤微环境引发炎症反应和肿瘤负荷短暂增加所导致,其实并不是真正意义上的肿瘤进展。
影像学表现:肿瘤体积的增大或出现新发病灶,一段时间后肿瘤体积开始缩小;
病理活检结果:免疫细胞如细胞毒性T淋巴细胞等对肿瘤细胞的炎症浸润、水肿、坏死,同时较少伴有临床症状。
3.2关于超进展与假性进展的鉴别
目前,区分假性进展和HPD的时间是8周,通常使用纵向影像学监测和反复病理活检进行鉴别,也可根据临床症状辅助鉴别。
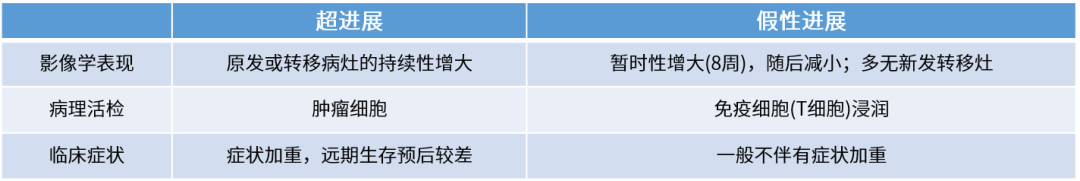
利用生物标志物检测进行鉴别的方式也逐渐得到重视。
研究发现,125例接受ICIs治疗的黑色素瘤患者中ctDNA预测假性进展的敏感性为90%(95% CI:68%~99%), 特异性为100%(95%CI:60%~100%)。假性进展患者的ctDNA水平呈现迅速且显著下降,而真正发生进展患者的ctDNA水平会明显升高。另外,在一个15例的多癌种队列中观察到ctDNA变化与OS期之间存在相关性。
由此可见,ctDNA可能是鉴别肿瘤假性进展的潜在生物标志物,有待在前瞻性大样本研究中进一步验证。
Part4
总结与展望
免疫治疗的出现已经改变、并且还将继续改变恶性肿瘤的治疗格局,同时免疫治疗的“Dark Side”也是不可忽视的。有10%左右的患者在使用ICIs后出现超进展(HPD),HPD的发生通常意味着更快的疾病进展和更短的生存预后,这给ICIs的临床应用带来一定困扰。
目前,HPD的评估标准不统一,现有评估肿瘤生长速度的两个指标TGK和TGR的计算依赖于治疗前后完整的影像学资料,导致评估的准确性受限。HPD发生的潜在机制仍不清楚,研究显示HPD的潜在发生机制与肿瘤的免疫微环境变化、致癌信号的激活和促肿瘤细胞因子的调节有关,具体机制仍有待在大样本人群中进行验证。HPD预测因素的研究处于初步研究阶段,研究显示高龄、肿瘤区域复发、MDM2/4扩增和EGFR突变可能与HPD发生有关,但是仍存在不同研究结论相悖的情况。而且现有HPD的研究多为小样本回顾性研究,尚缺乏前瞻性大样本研究进行探索和验证,存在一定局限性。
免疫治疗超进展是需要被正视的客观问题,但不应当让它成为掣肘免疫治疗应用的原因,所以,如何减少HPD对患者造成的损害成为亟待解决的问题,找到可以早期识别和预测HPD发生的生物标志物是关键。肿瘤免疫微环境检测以及基于NGS技术的液体活检已经在HPD预测中显示出初步价值,能在一定程度上弥补影像学检查的不足,并实现动态监测。
未来,期待基于NGS的肿瘤微环境检测和液体活检技术助力优化免疫治疗的使用,使免疫治疗造福更多能从中获益的患者。
臻和基因 平台发布
查看更多