查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





患者男,58岁,因“头晕5天”就诊。
现病史:患者近5日无明显诱因出现头晕,呈昏沉感,阵发性,持续时间约大半天,无伴有肢体乏力、恶心、呕吐、视物模糊、听力下降、耳鸣、冷汗、吞咽困难、构音障碍等不适,为求进一步诊治,于我院就诊。
既往史:6年前发现血糖升高。空腹血糖波动在6.2-7.1 mmol/L,餐后血糖波动在12-14 mmol/L,无多饮、多食、多尿、消瘦。高血压病史3年。乙肝病毒携带者病史30余年,丙肝病史30余年,家族史:否认家族中类似疾病患者。
个人史:否认吸烟、饮酒史。
体格检查:神志清,对答切题,双侧瞳孔等大等圆,直径约3mm,直接、间接对光反射灵敏,眼球各向运动到位,鼻唇沟对称,伸舌居中,双侧肌张力正常,左侧肢体肌力5级,右侧肢体肌力5级,深浅感觉对称存在,四肢腱反射活跃,颈软,双侧病理征阳性。体型偏瘦,无紫纹、黑棘皮,腹软,无压痛及反跳痛,未触及肿物,双肺呼吸音清,未闻及干湿啰音,心率齐,未闻及病理杂音。
辅助检查:糖化血红蛋白6.5%,血脂稍高,同型半胱氨酸偏高,其他常规及相关检查无明显异常。2013-2021年多次头颅磁共振检查显示,半卵圆中心多发扩大的血管周围间隙(PVS)、斑点状白质高信号(WMH)逐渐增多,白质病变加重,且2016-2021年间出现多次脑出血。

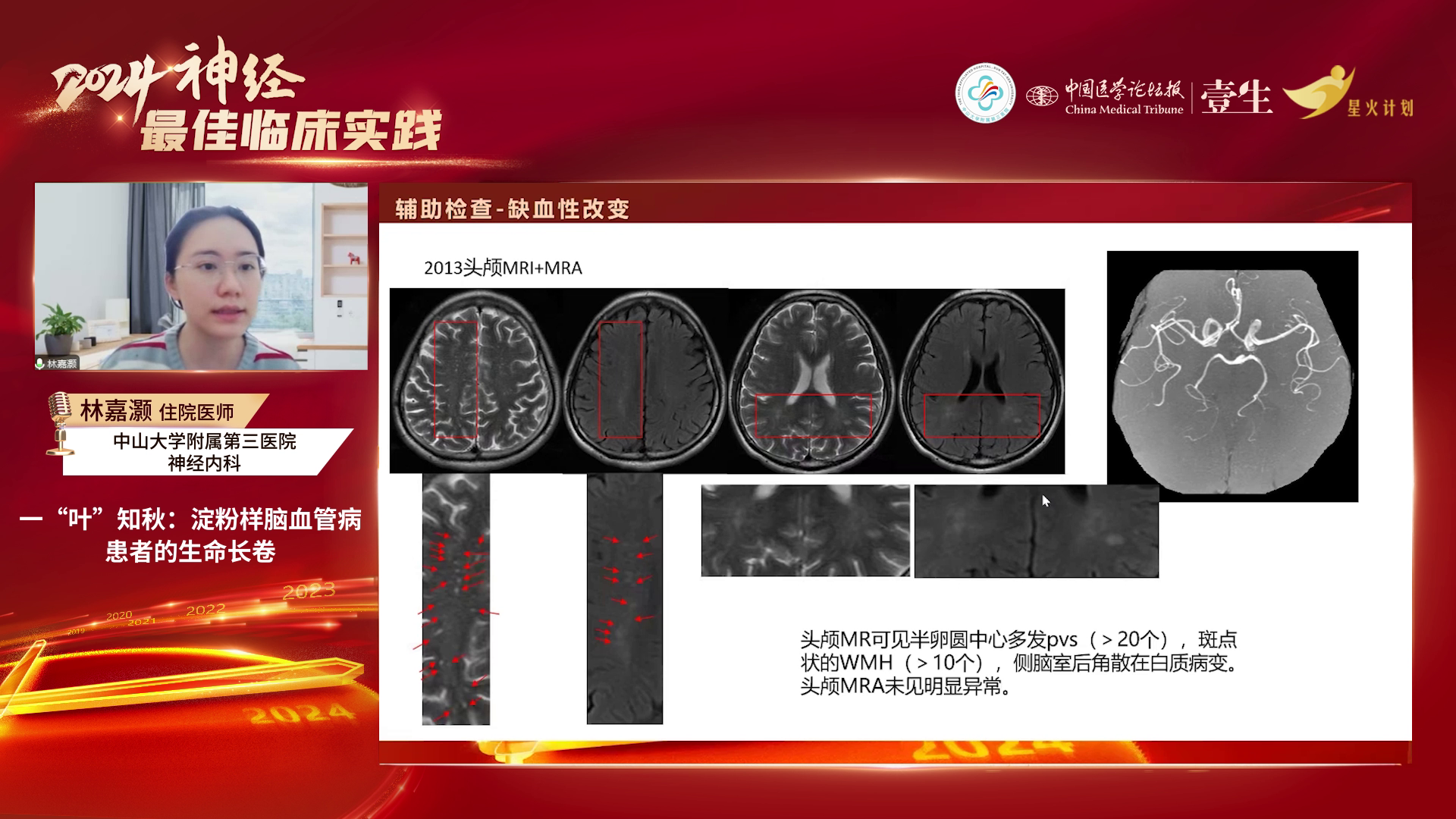
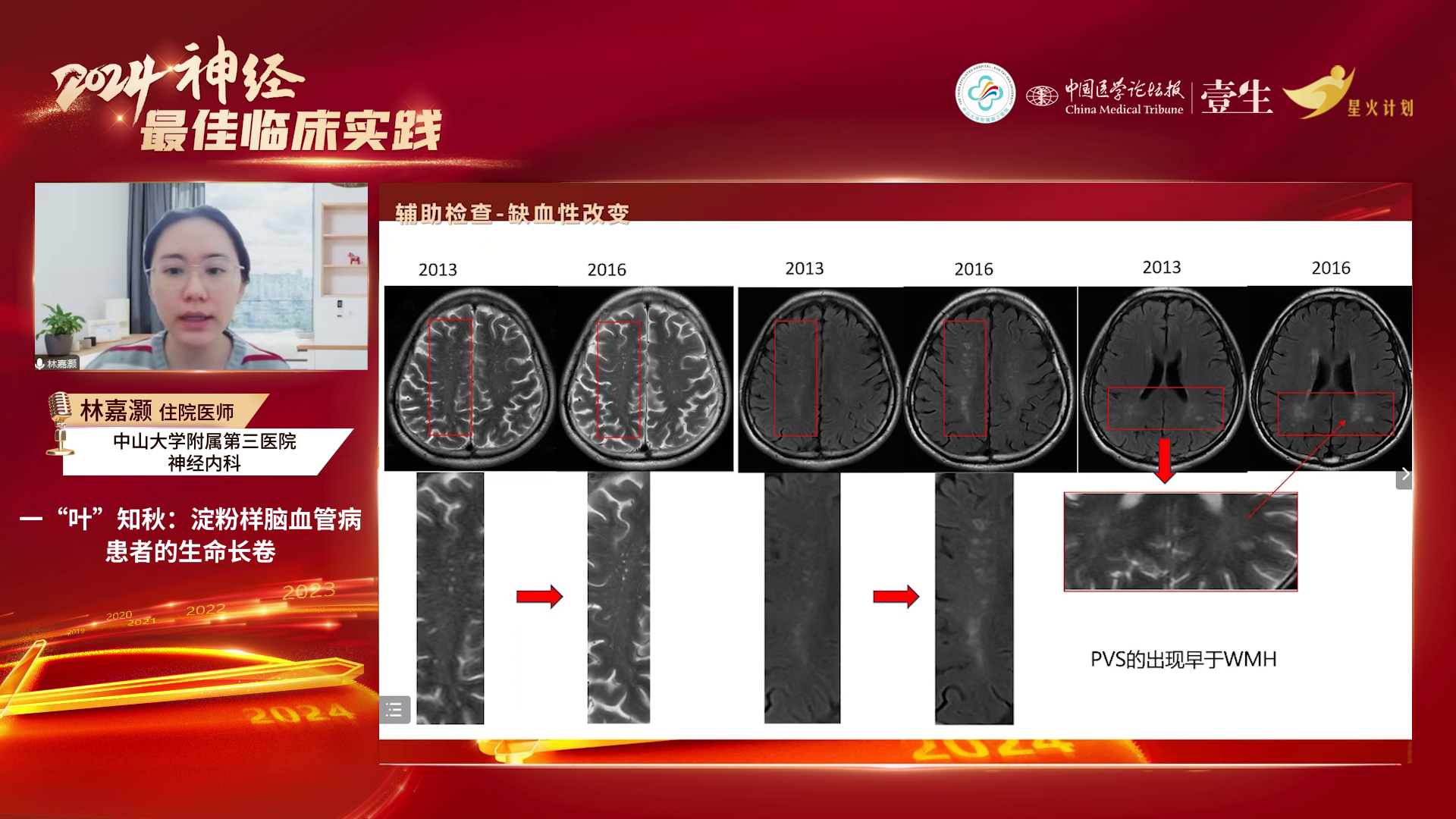
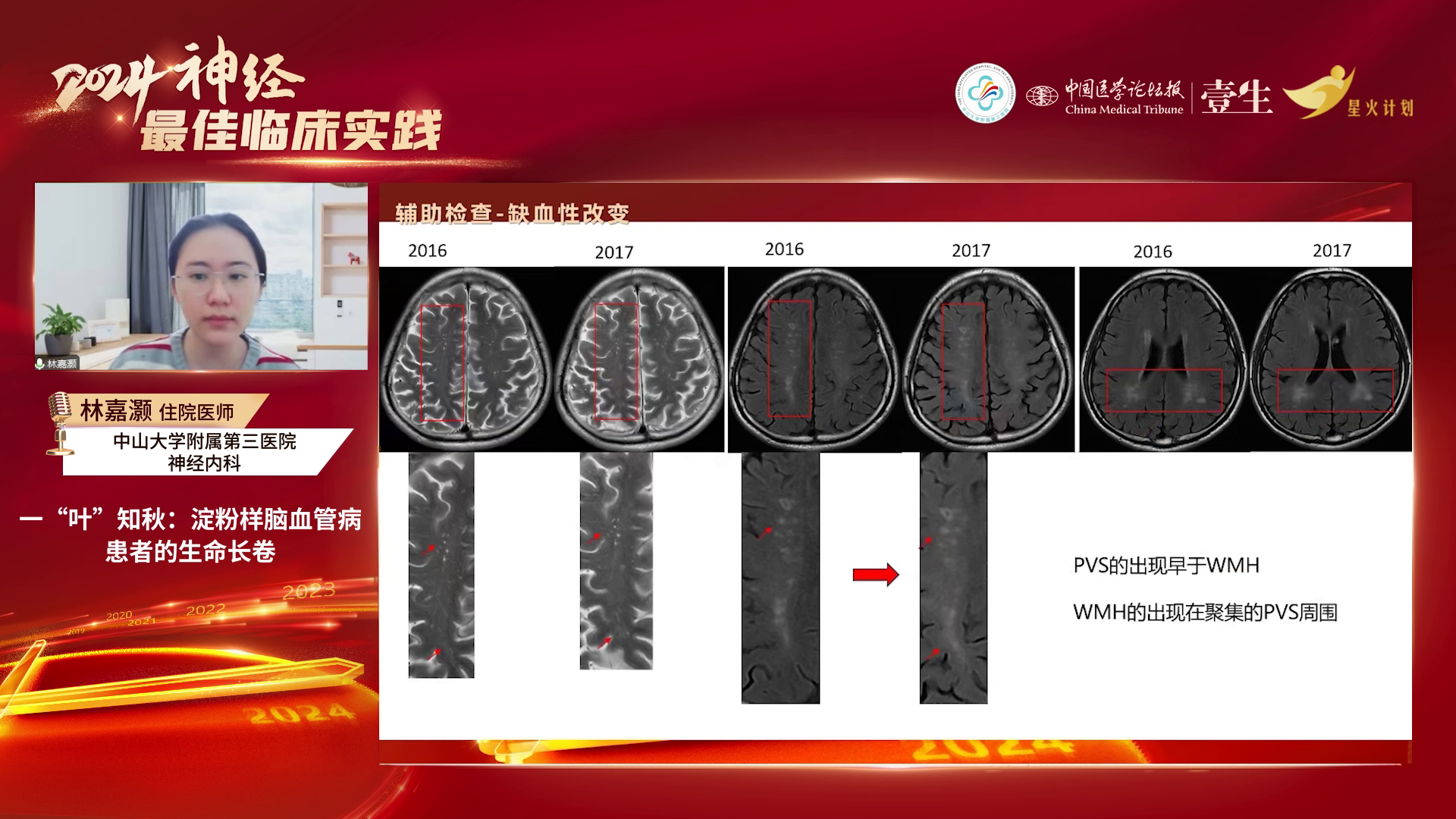

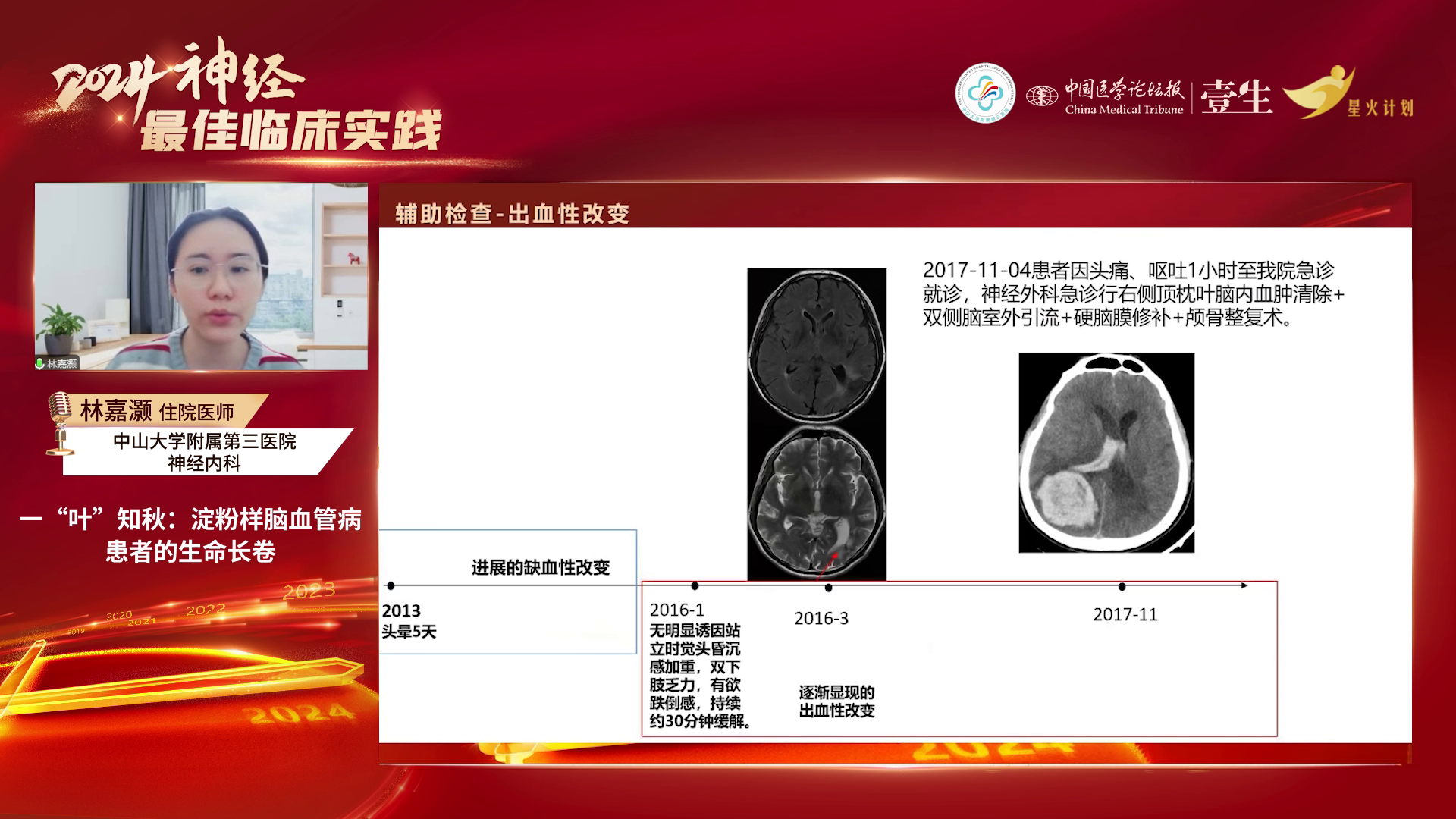
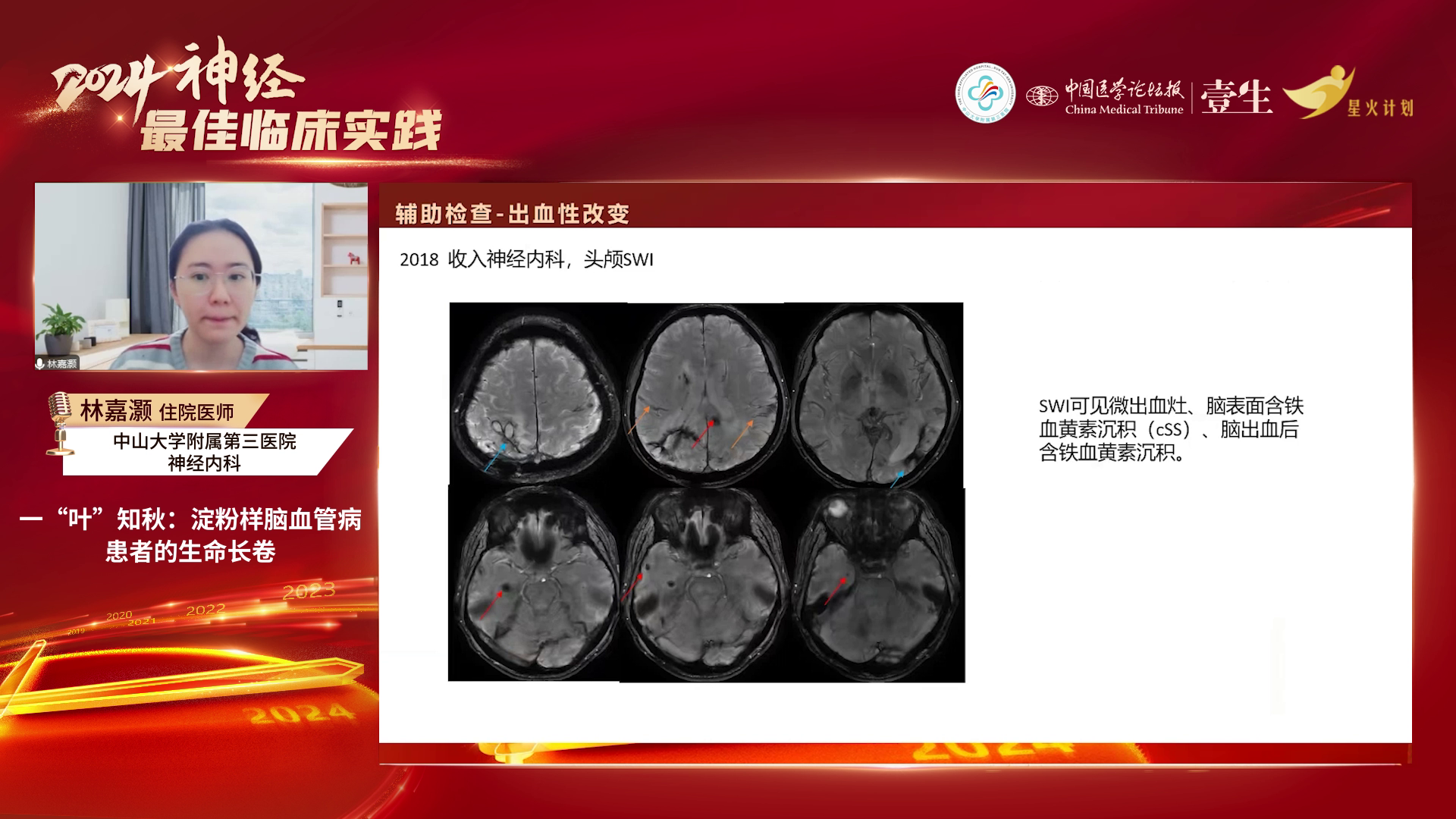
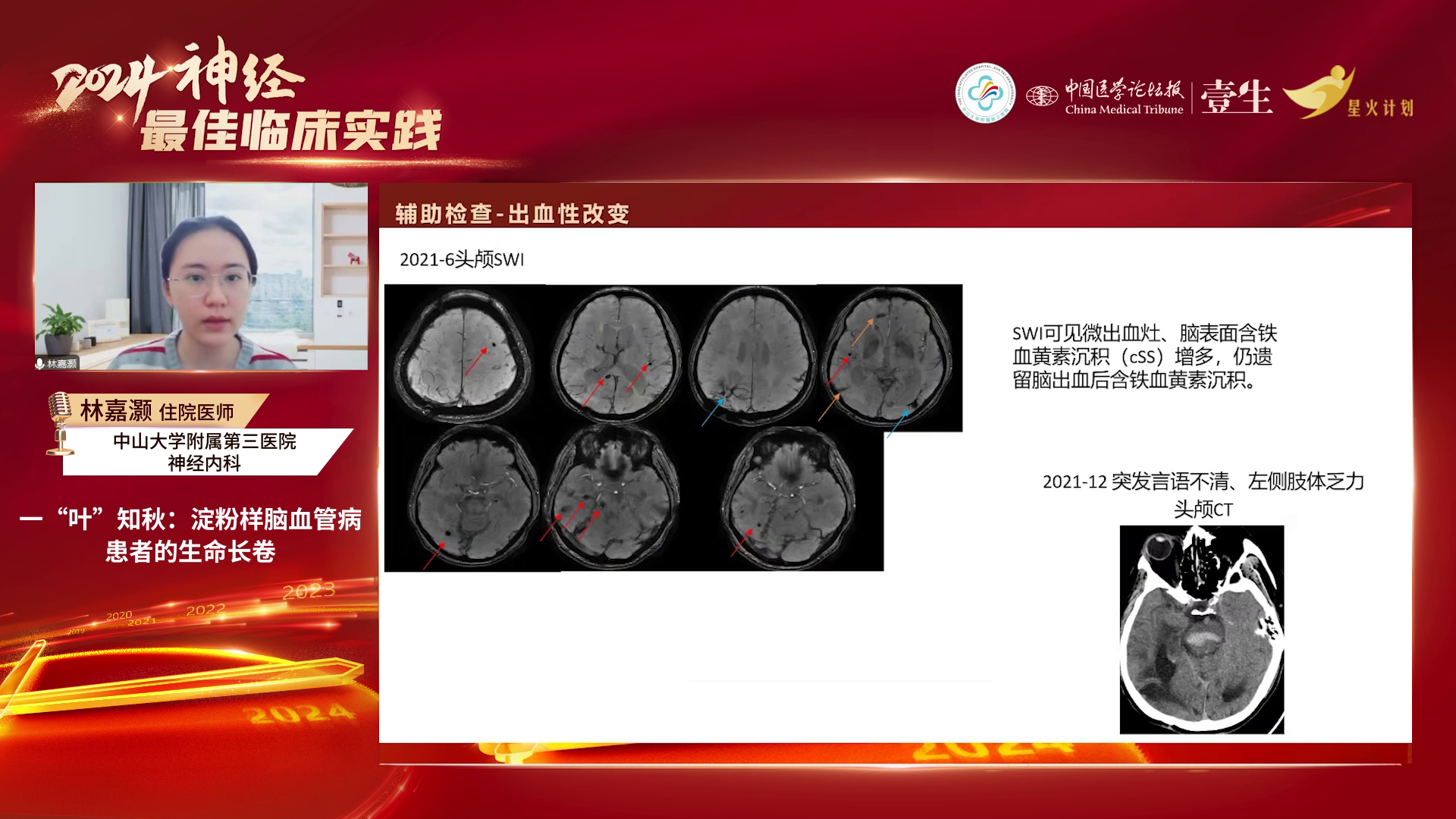
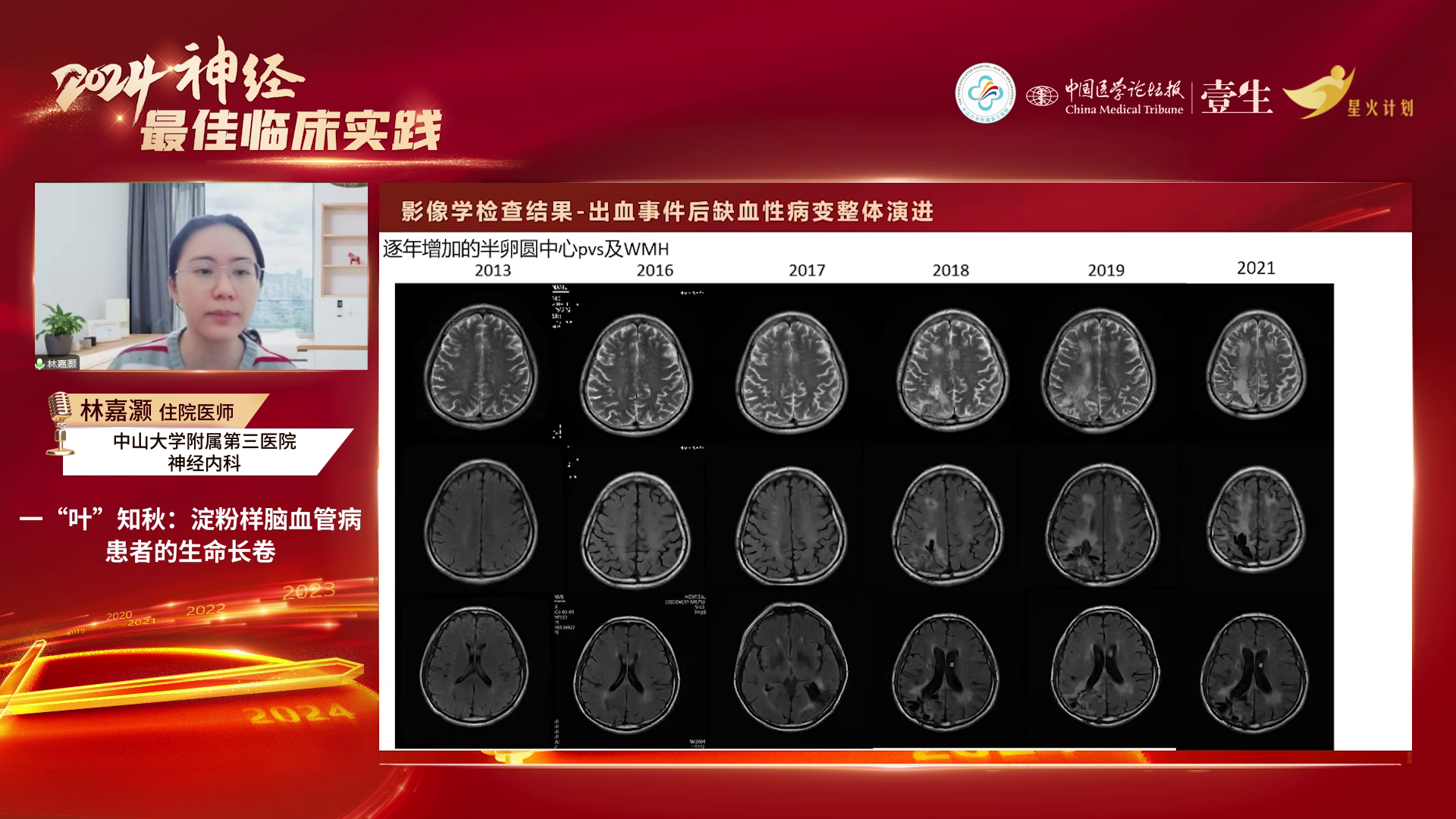
疾病进展:2016年1月患者头昏沉感加重、双下肢乏力;2016年3月发现无症状性左侧脑室脑出血;2017年11月右侧顶枕叶出血破入脑室,行颅内血肿清除术;2018年发现脑出血后含铁血黄素沉积及脑表面含铁血黄素沉积、多发脑叶微出血灶;2021年12月脑叶出血致言语不清、左侧肢体乏力,最终于2024年死于肺部感染。
1)诊断:考虑淀粉样脑血管病(CAA)。支持证据包括患者有症状性脑叶自发性脑出血,影像学提示多次自发性脑出血、脑叶多发微出血灶、半卵圆中心多发epvs(>20个)及多发斑点状脑白质高信号(>10个),患者年龄大于50岁。
2)鉴别诊断
CADASIL:临床表现异质性高,包括偏头痛、多发卒中事件、认知障碍、步态障碍等。磁共振可见多发腔梗、白质病变以前部为主,有特异性外囊白质病灶及颞极对称白质病灶,基因检测可发现NOTCH3基因突变。在东亚人群中约25%患者可表现为出血性卒中事件。
动脉硬化性脑小血管病:缺血病灶以基底节区周围对称性为主,呈额叶优势或前后对称分布,基底节区常见多发PVS,出血性改变以混合微出血灶为主,颅内出血少见。
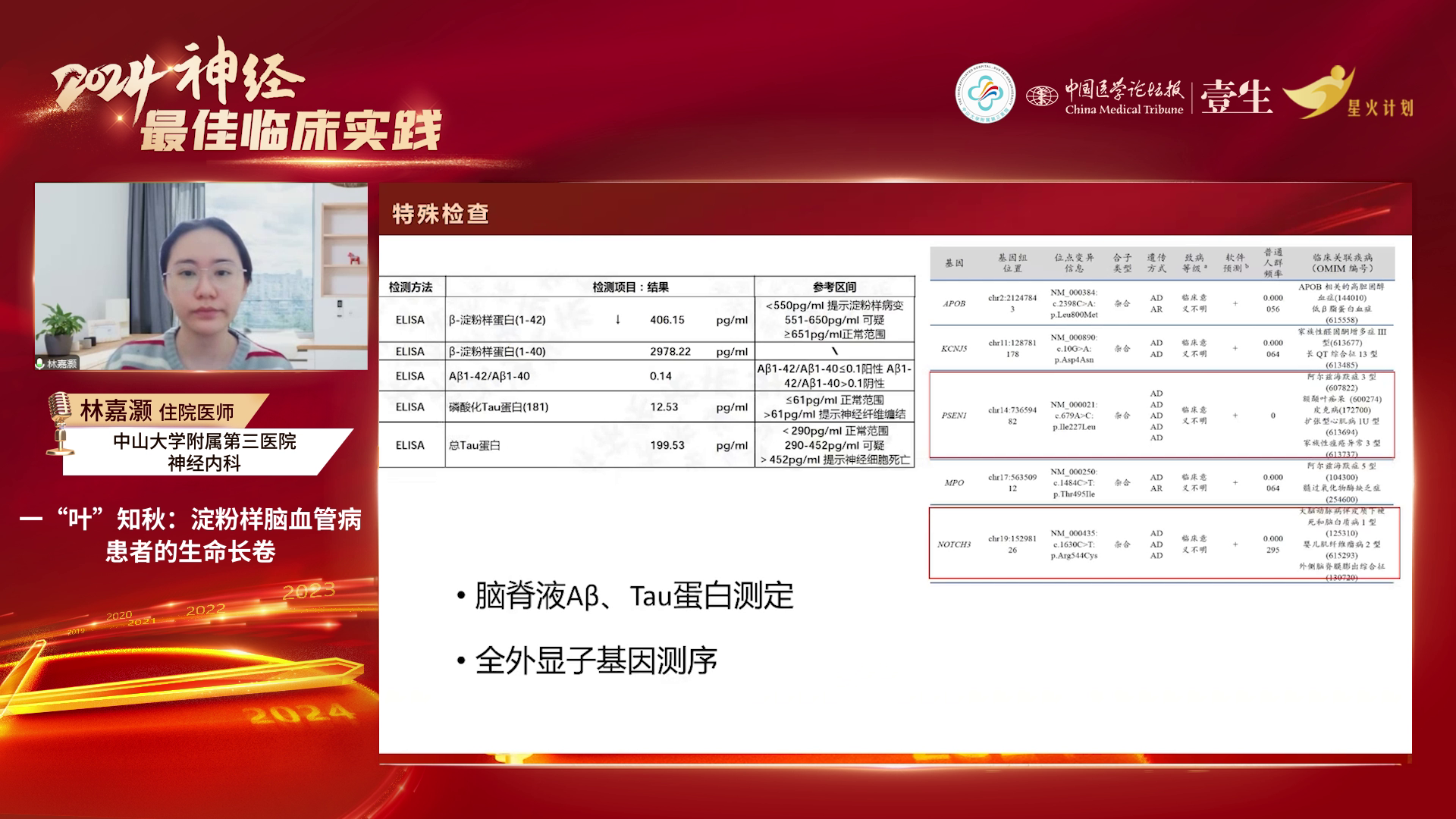
3)最终诊断:结合波士顿2.0诊断标准及患者影像学结果,考虑诊断为很可能淀粉样脑血管病。同时患者脑脊液Aβ42水平下降,全外显子基因测序发现与Aβ代谢相关的PSEN1基因突变、NOTCH3基因突变。
1)急性期治疗:自发性脑出血急性期,外科治疗远期获益尚不明确,内科治疗中早期强化降压、血糖控制、体温管理及凝血状态管理可能有帮助。

2)二级预防:重点控制血管危险因素,如高血压与糖尿病。非药物治疗包括体育锻炼、社会活动和生酮饮食等。

3)特殊情况决策
溶栓治疗:CAA患者溶栓需谨慎,高龄患者、脑微出血存在及负荷与溶栓后症状性出血风险显著相关,1-10个脑微出血灶视为静脉溶栓相对禁忌。大血管闭塞急性缺血性卒中患者中,CAA患者血管内治疗后90天良好预后率更低,血管内治疗前接受溶栓者可能获得更好预后。
抗血小板与抗凝治疗:复发性颅内自发性脑出血患者中,阿司匹林应用、既往脑出血病史后部CT的GRE序列两个以上微出血灶与脑出血复发风险增加独立相关,抗血小板药物使用应谨慎。房颤患者口服抗凝药进行卒中预防应避免用于可能及确诊的CAA患者,达比加群酯可能减少颅内出血风险但未被大样本证实,高出血风险CAA患者合并房颤,左心耳封堵术可能合理,所有决策应遵循临床医生与患者共同决策模式。
查看更多
专家点评
本例患者临床表现并不典型,既无脑出血、认知障碍,也无典型CAA特征,而是以短暂性局灶性神经功能障碍为主,无癫痫发作。其早期临床特点为五十多岁时(2011年)出现头昏沉感,属于非出血性症状。影像学早期标志物也非脑出血或脑表面含铁血黄素沉积,而是非出血性改变:一是半卵圆中心或皮质软脑膜下超过20个的PVS,二是顶枕后部脑白质高信号(WMH)在半卵圆中心呈斑点状、数量超过10个。这两个非出血影像标志出现较早,直至2017年患者发生脑叶出血才引起重视,经检查确诊为PSEN1基因突变的遗传性脑淀粉样血管病,同时合并NOTCH3基因突变。双基因突变均影响血管平滑肌功能,分别通过Aβ沉积与血管壁结构异常促使脑叶出血较早发生,提示应重视CAA非出血期的早期识别——当特定部位的PVS与WMH出现时需高度警惕。
此外,早期识别应结合病史与家族史评估,例如该例患者在发病前六年已患糖尿病,后者既是散发性CAA的危险因素,也可能与遗传背景相互作用。鉴别诊断需注意与CADASIL区分,后者出血灶多分布于基底节、脑干及小脑,而CAA相关出血以脑叶为主,二者亦可合并存在。
治疗方面需特别关注,对于高龄或存在缺血性卒中事件的患者,应评估是否合并CAA。若患者表现为轻度非致残性卒中(如NIHSS评分2-3分)且伴有糖尿病等CAA危险因素时,溶栓治疗属于禁忌,因其可能诱发脑出血。同样,若需抗凝治疗(如合并房颤),也需谨慎评估出血风险,必要时考虑左心耳封堵术。综上,本次讨论强调了对CAA非出血期表现的早期识别与风险评估,以避免溶栓或抗凝治疗所致出血并发症,这对临床决策具有重要意义。