查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





病史摘要
56岁中年女性,主诉常规体检发现左肺下叶磨玻璃结节,随访增大。
初步诊断:早期肺癌。
诊疗过程:
(1)无手术禁忌,拟行手术治疗。
(2)术前评估
CT提示左肺下叶磨玻璃样结节,轴位最大径1.1cm,矢状位最大径1.6cm。结节内可见实性成分,实性成分占比约25%,诊断早期肺癌,手术指征明确,拟行解剖性部分肺叶切除术。
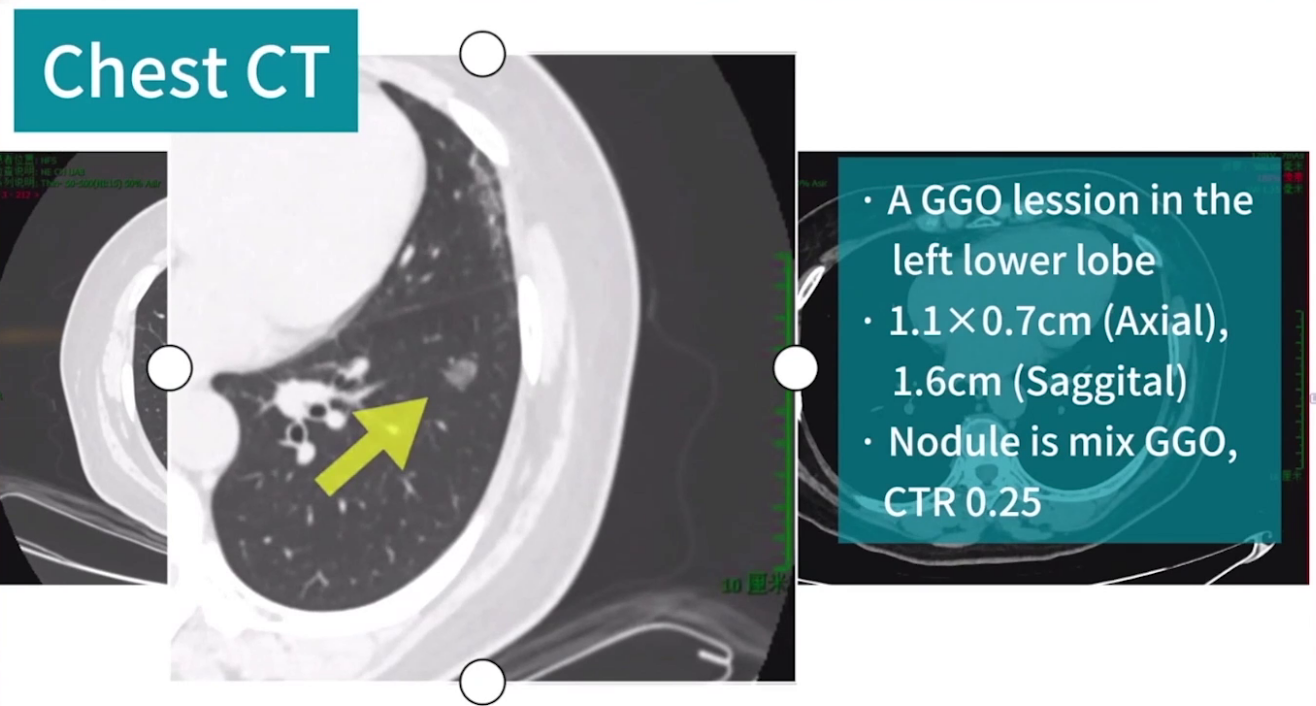
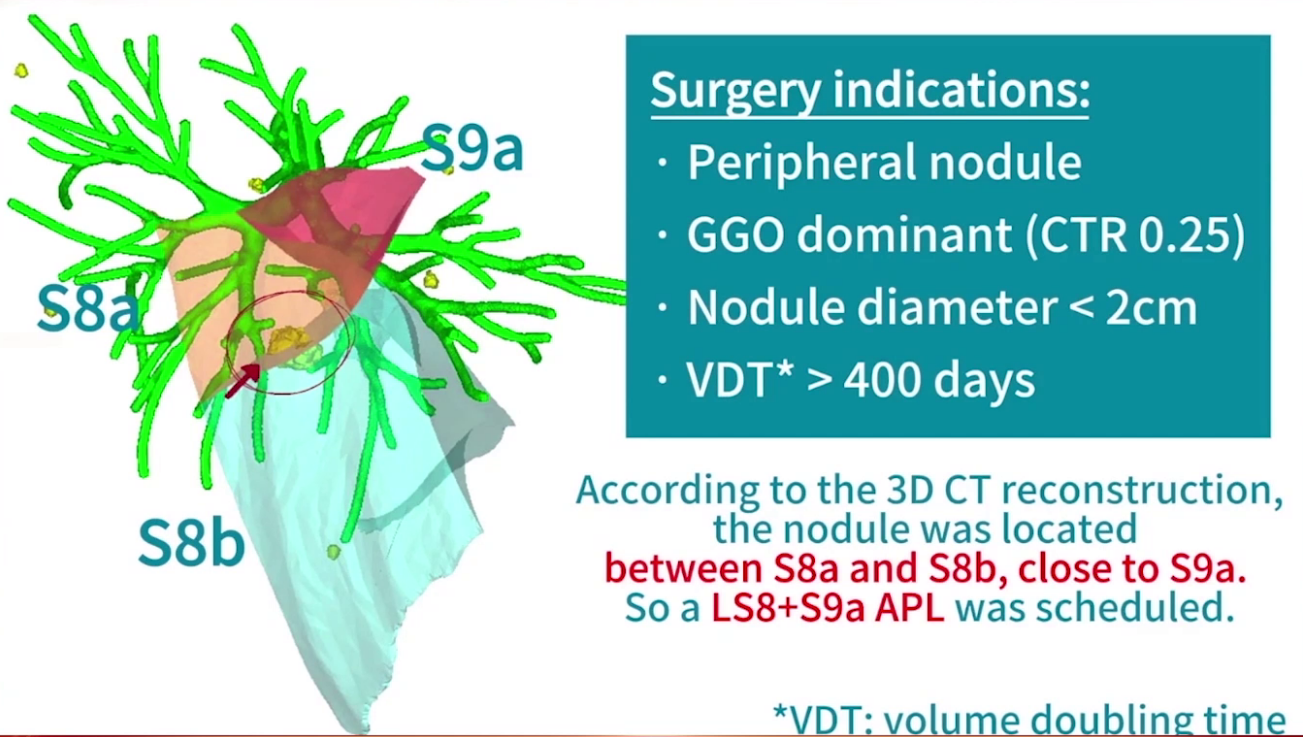
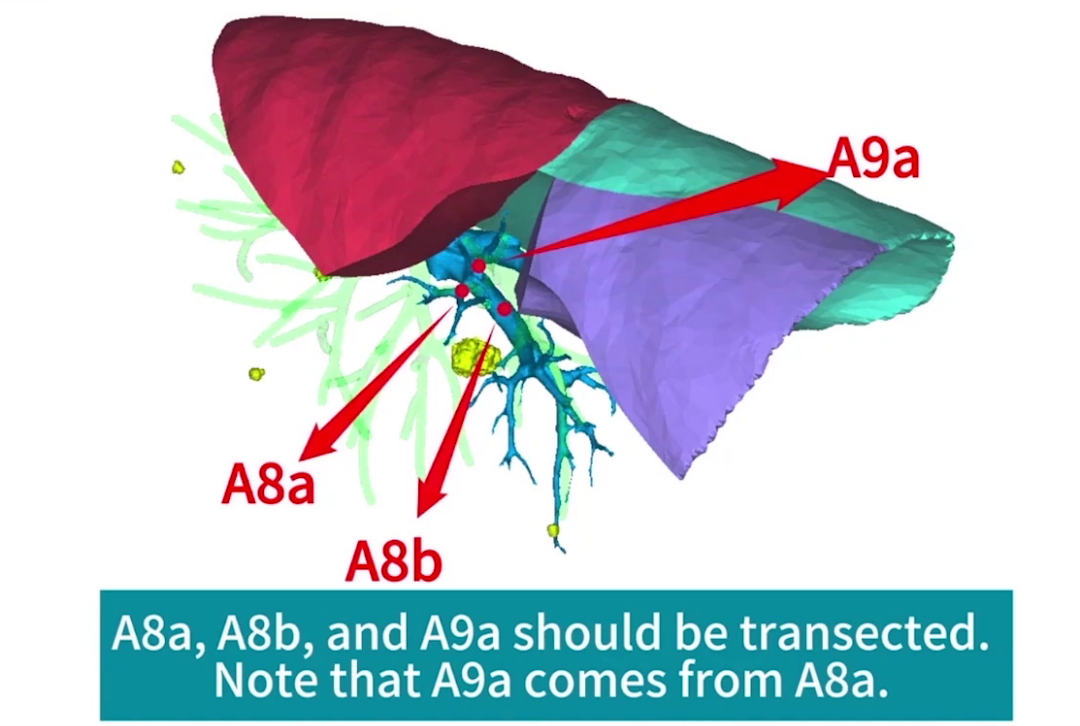
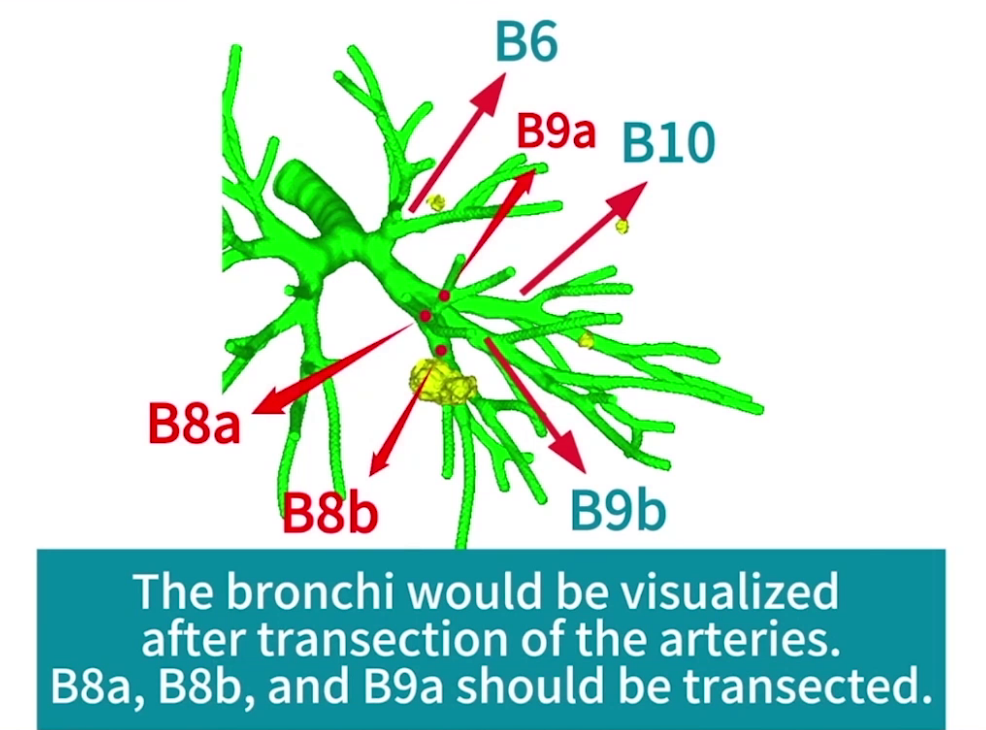
术前CT三维重建显示结节位于S8a及S8b之间,紧邻S9a,计划切除左下肺S8及S9a。切缘受累动脉包括A8a、A8b及A9a(A9a与A8a共干),受累支气管包括B8a、B8b及B9a,需切断。V8a作为S8a与S8b段间静脉,需切断,V8b接受S8b静脉回流分支,需切断。
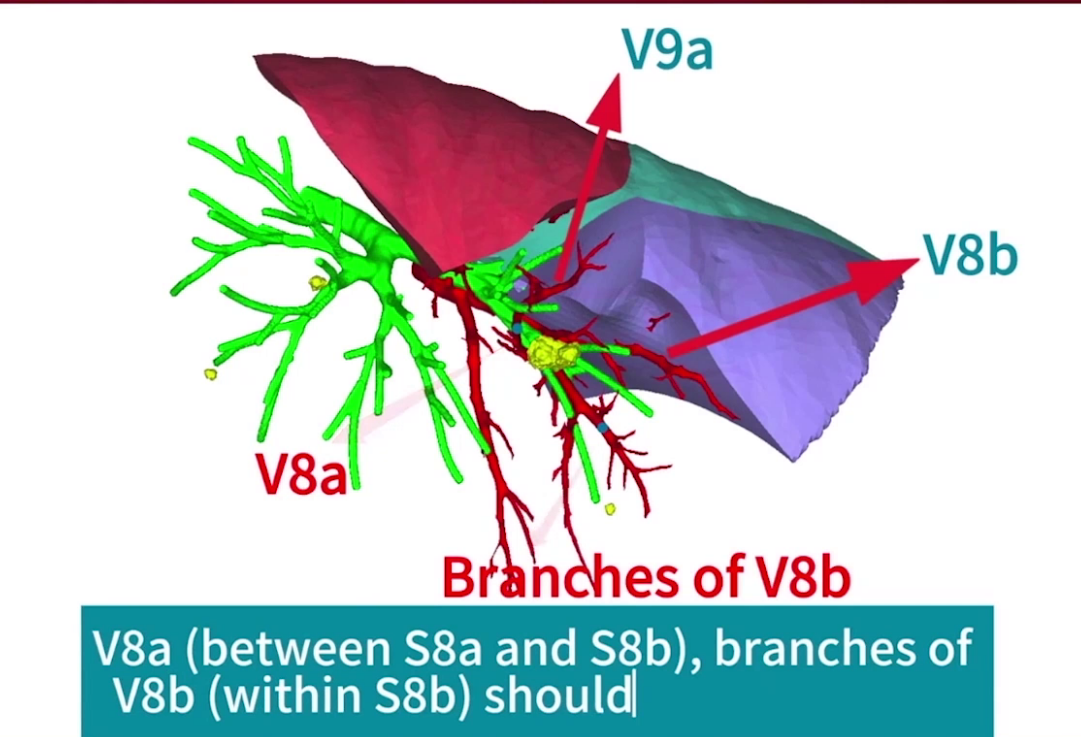
(3)手术治疗(完整解析详见病例视频)

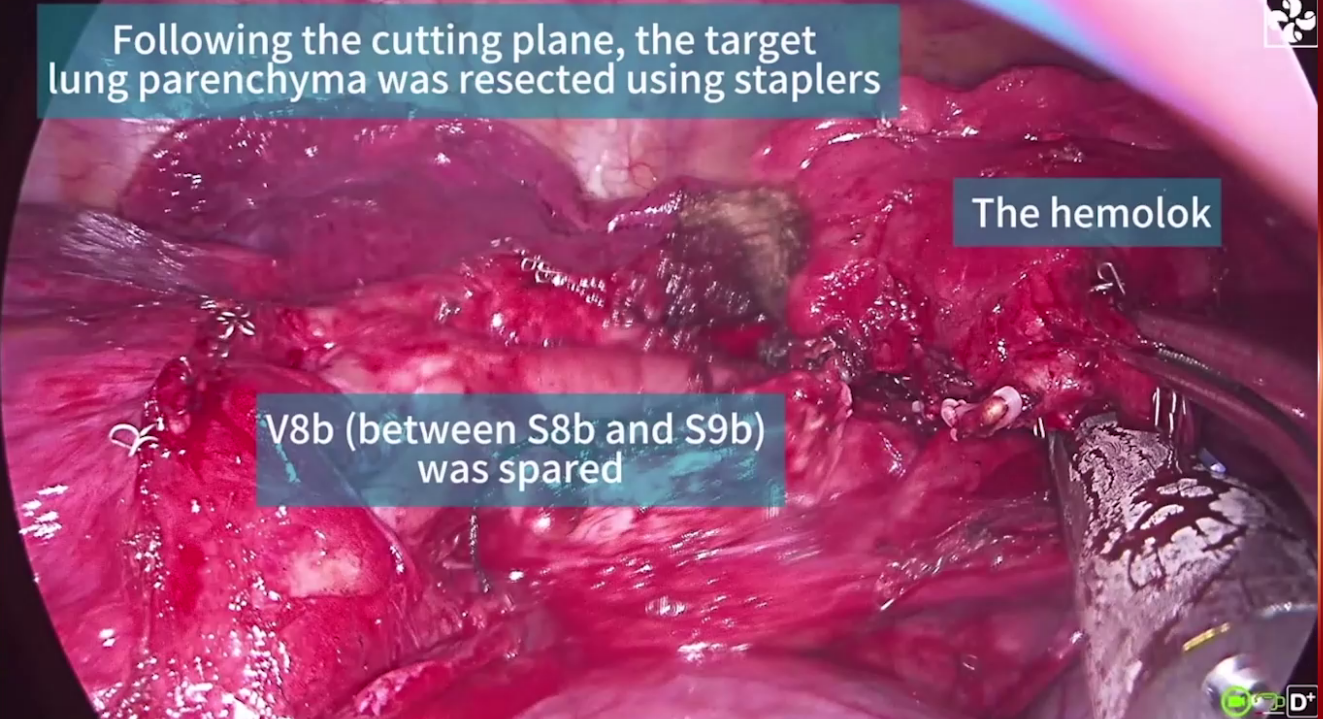
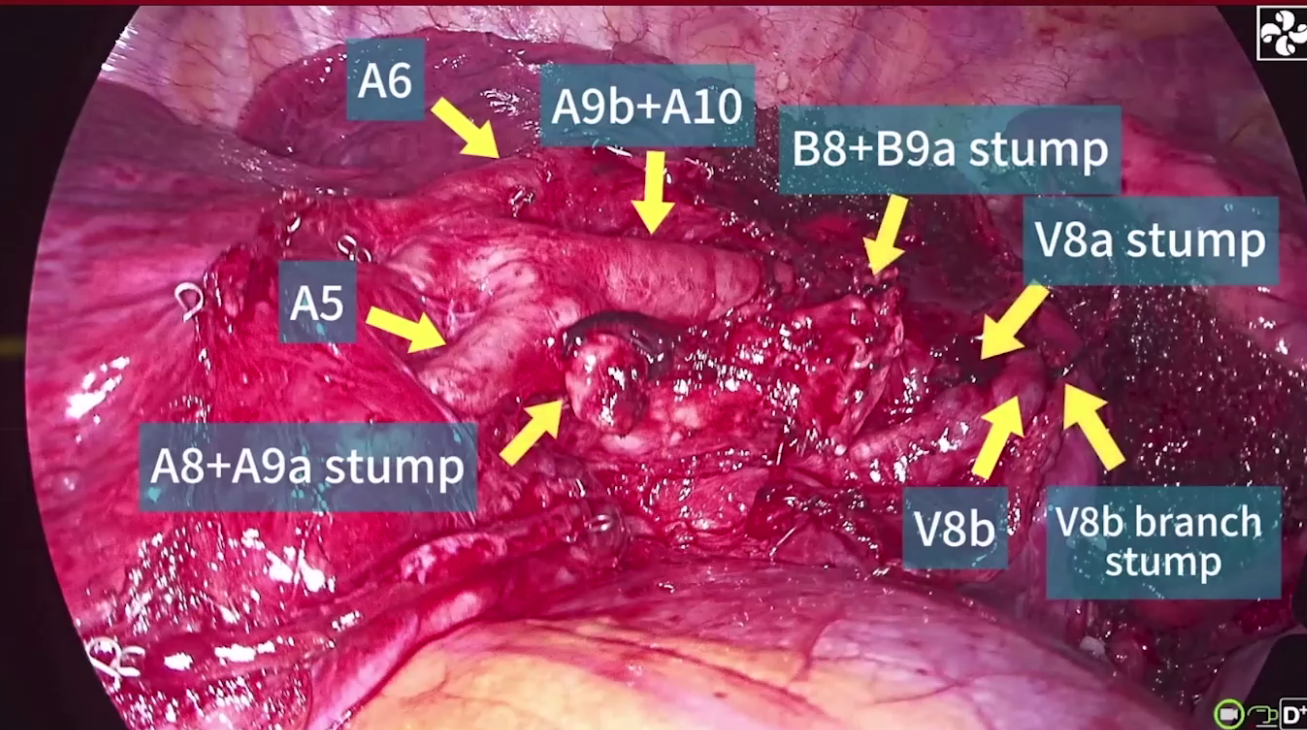
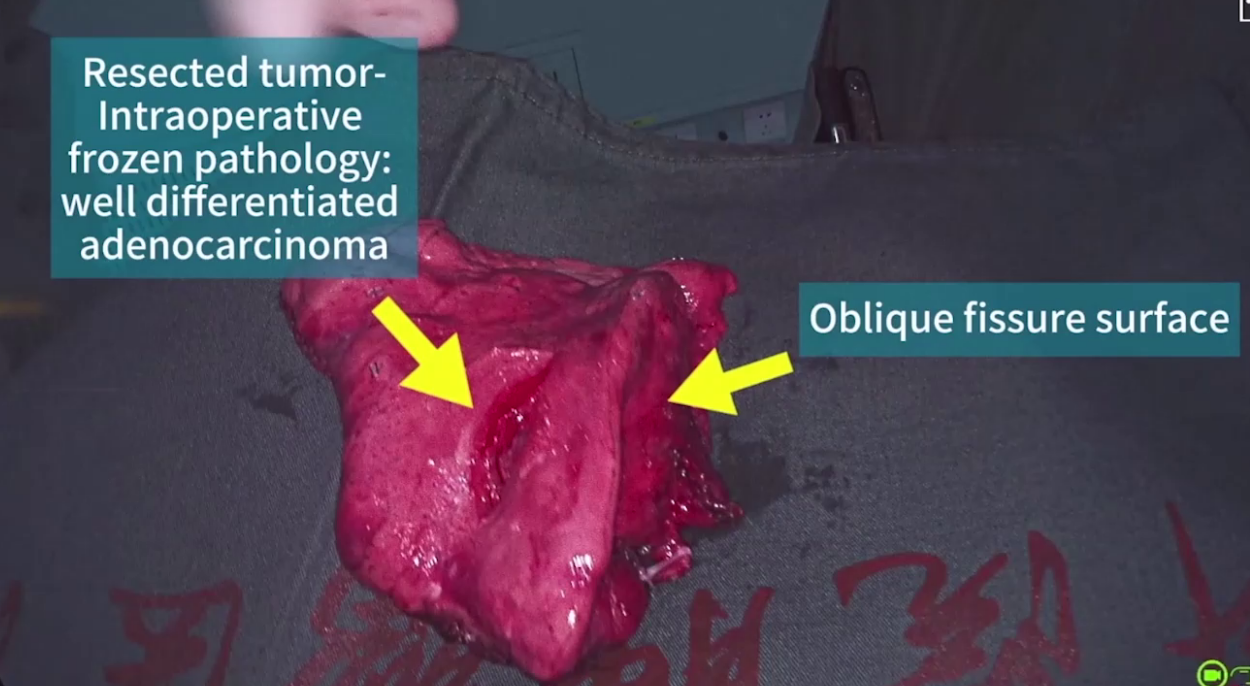
(4)术后管理
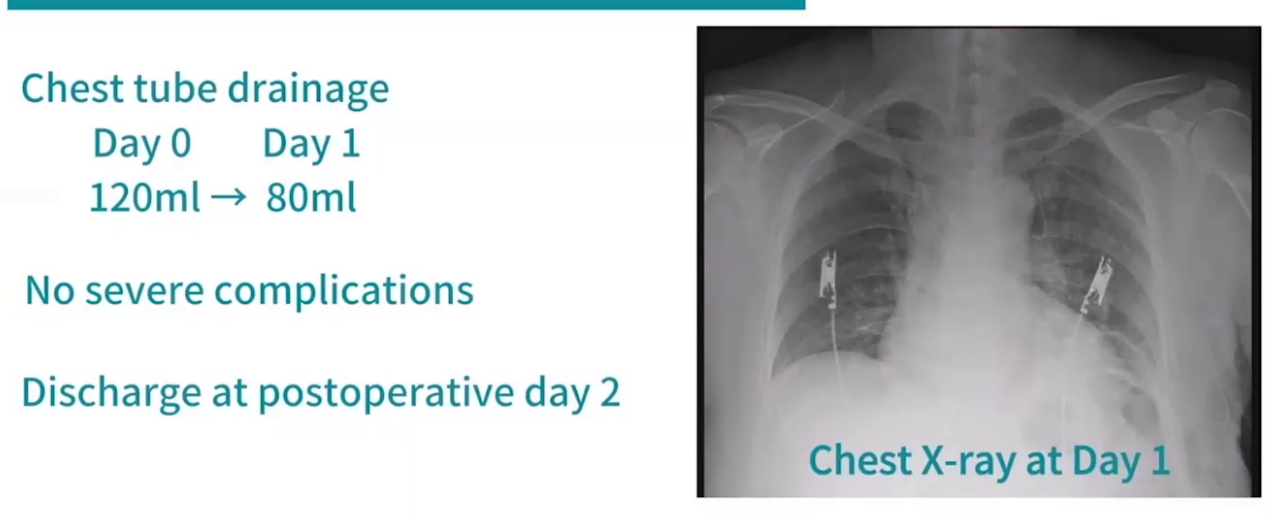
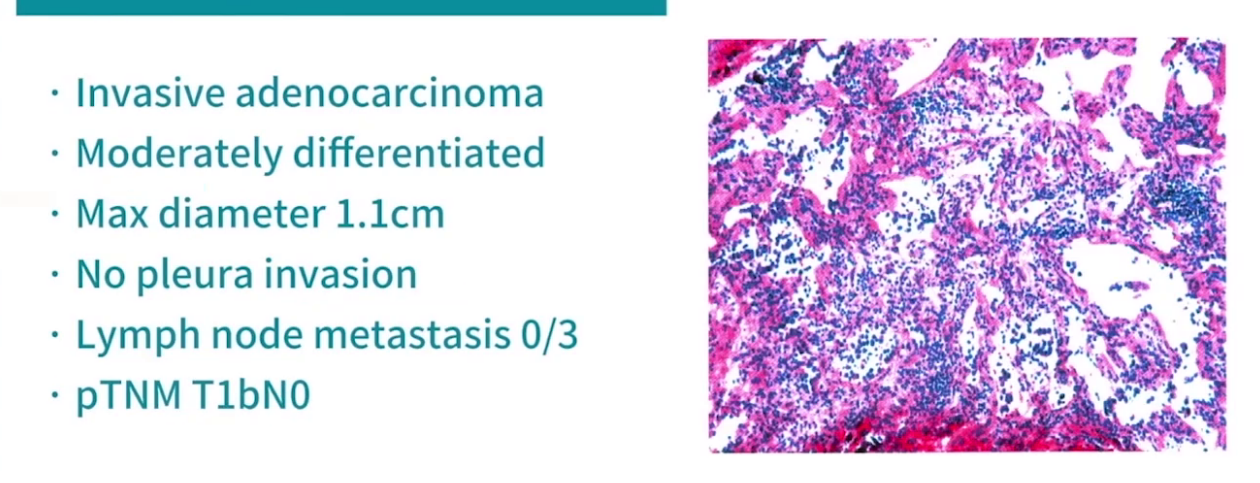
患者术后引流不多,未出现严重并发症,术后第一天胸片正常,术后两天拔管出院,手术病理提示中分化浸润性肺腺癌,淋巴结未见转移,分期T1bN0,术后无需辅助治疗,定期复查。
1.早期肺癌外科治疗发展进程
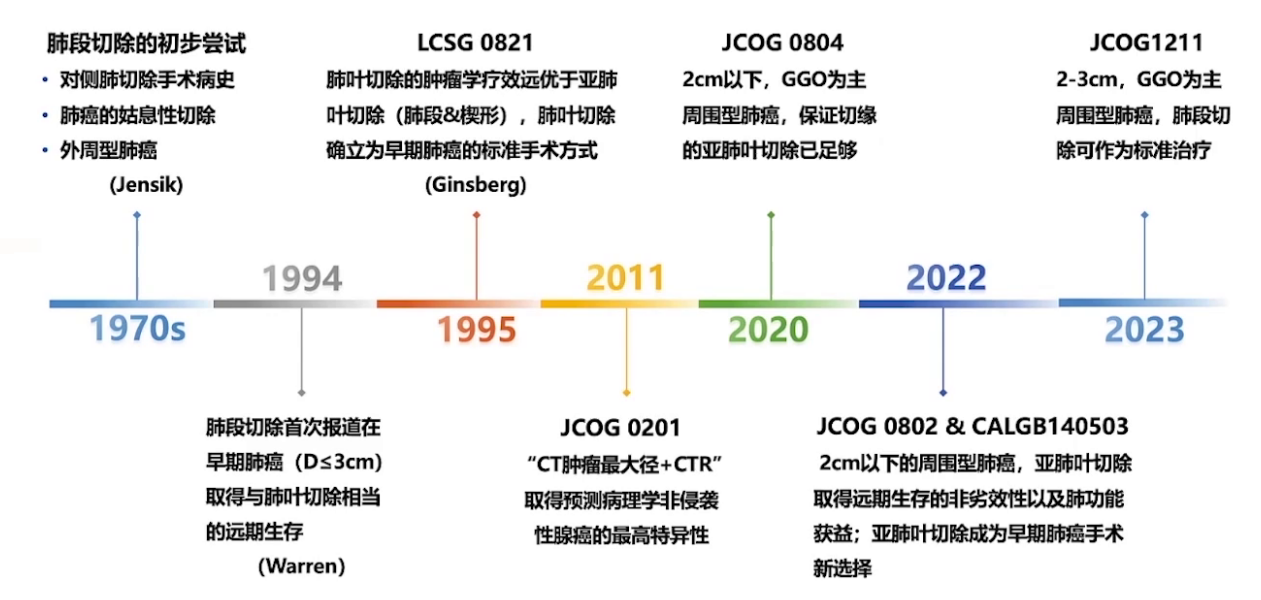
肺癌治疗中,亚肺叶切除的早期经验可追溯至20世纪70年代。1973年,芝加哥圣路加医学中心的Dr.Y报道了15年间肺段切除术治疗结局,周围型早期肺癌根治性肺段切除组五年生存率达56%,引发学界对肺段切除治疗早期肺癌可行性的探讨,保留肺功能成为选择亚肺叶切除的初衷。
1994年,Dr.Warren研究表明早期肺癌行肺段切除术可获与肺叶切除相似远期生存。
1995年,Doctor Ginsberg报道的前瞻性随机对照研究证实,即便早期周围性肺癌,肺叶切除术仍是首选。
2011年,日本JCOG 0201研究通过长期随访,发现CT影像特征可作为早期肺癌非浸润性的预测指标,将早期肺癌分为非浸润性与浸润性肺癌。
2020-2023年,日美研究者开展系列前瞻性干预性研究,如JCOG 0804、JCOG 1211、JCOG 0802以及CALGB 140503等,最终证实经适当筛选的早期肺癌,亚肺叶切除可行。
2.亚肺叶切除的早期经验
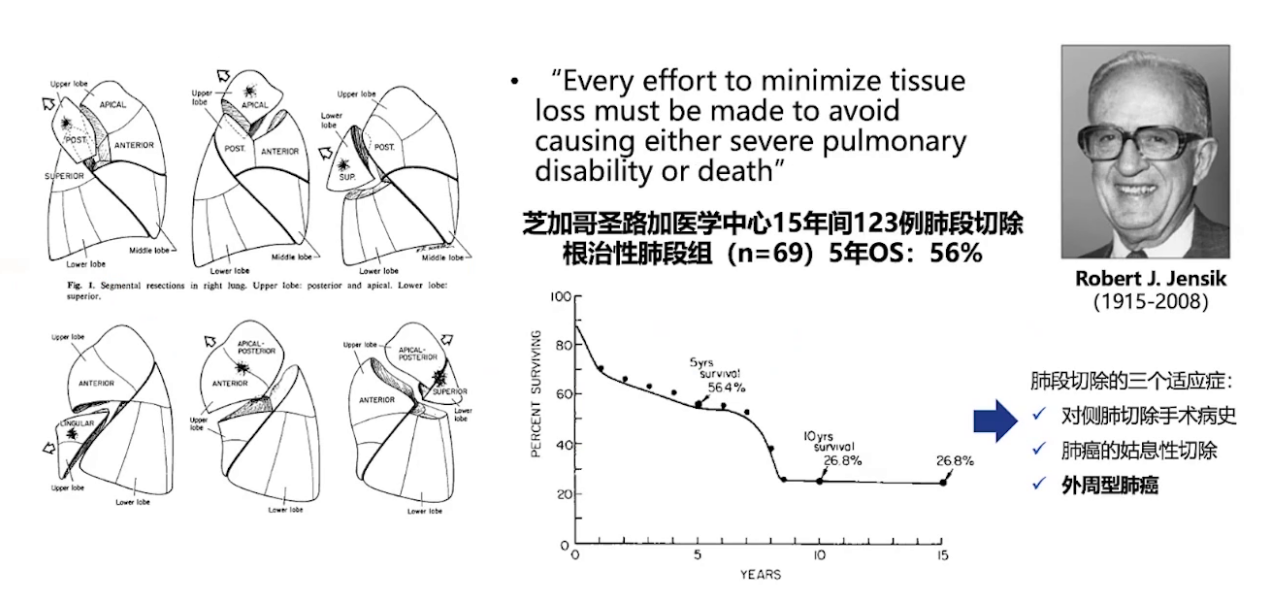
Robert J. Jensik认为肺段切除需尽量减少组织损失以避免严重肺功能障碍或死亡,芝加哥圣路加医学中心15年间123例肺段切除中,根治性肺段组(69例)的5年总生存率为56%、10年为26.8%。
肺段切除的适应证:对侧肺切除手术病史;肺癌姑息性切除;外周型肺癌。
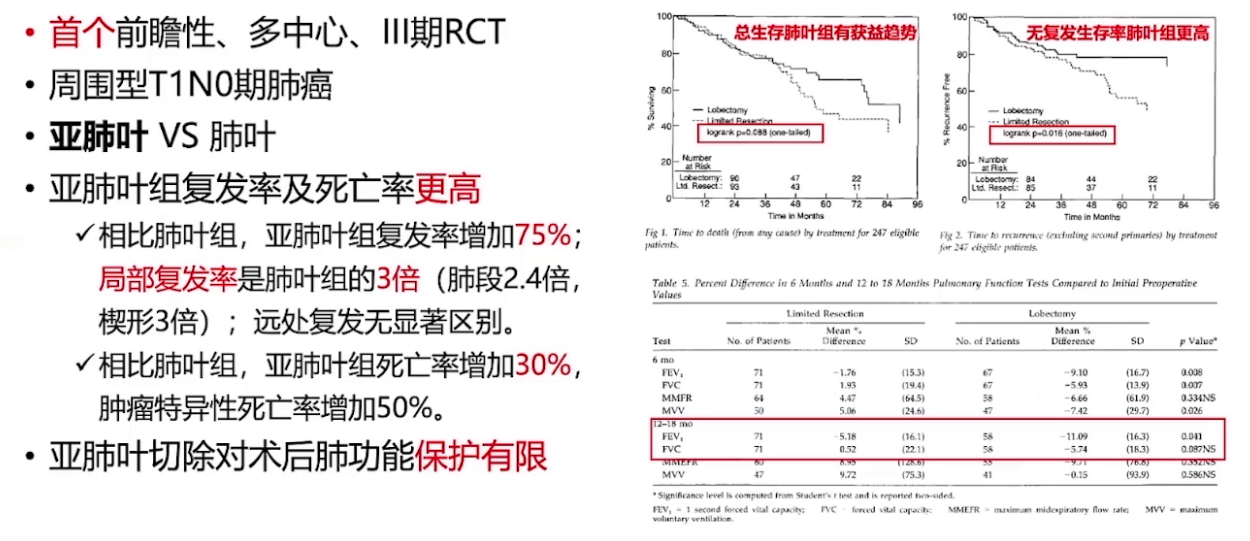
3.LCSG 821:肺叶切除术确立为周围型T1N0肺癌标准术式
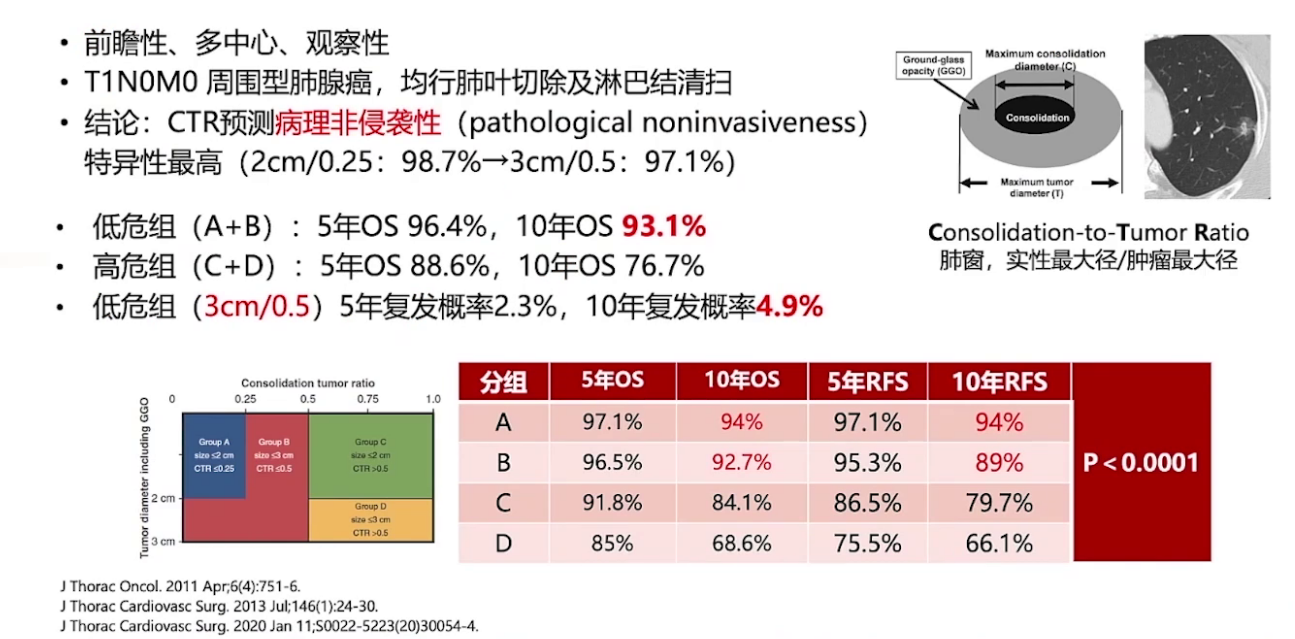
4.JCOG 0201:确立基于CT特征的早期肺癌分型体系
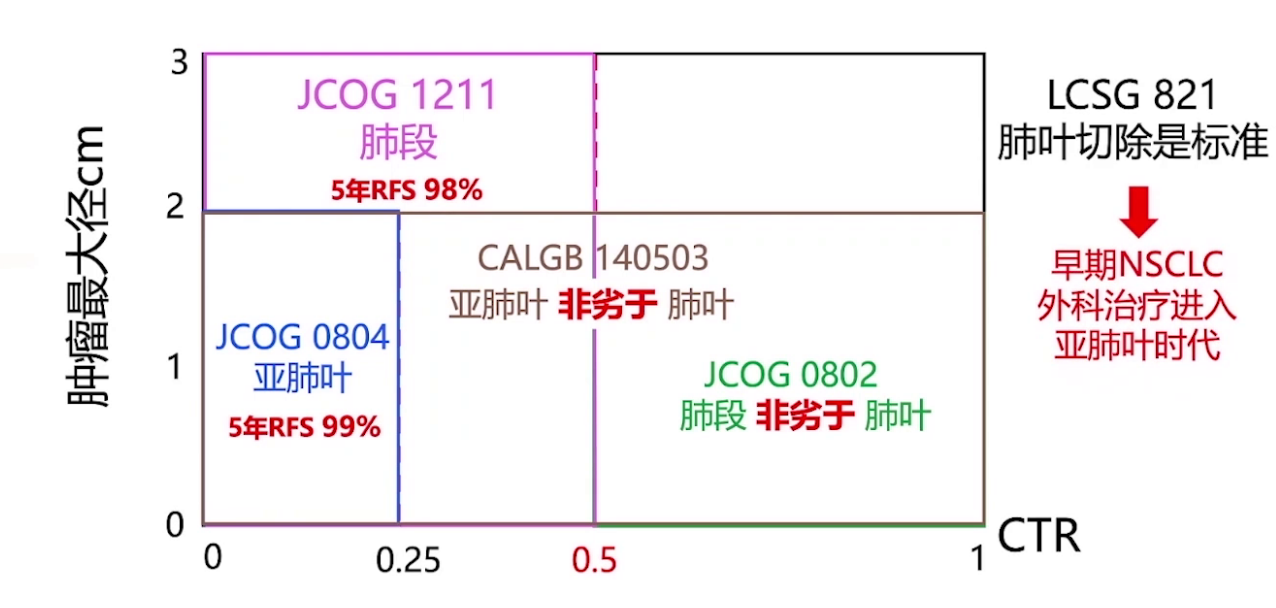
5.后821时代:亚肺叶切除探索三十年
 解剖性部分肺叶切除术
解剖性部分肺叶切除术
2014年,高树庚教授原创性提出解剖性部分肺叶切除术(APL)理念。APL依据肺组织气血双重供应解剖特点,以肿瘤学原则为基础,以保留更多健康肺组织为目的,基于肺段解剖结构进行部分肺叶切除。依肺癌性质、位置、大小不同,APL包含多种术式。APL操作要求精确解剖处理需切除靶肺组织主要脉管结构,保障切缘距离与肺门淋巴结处理,不拘泥于实际段间交界,不强求保留段间静脉全程。
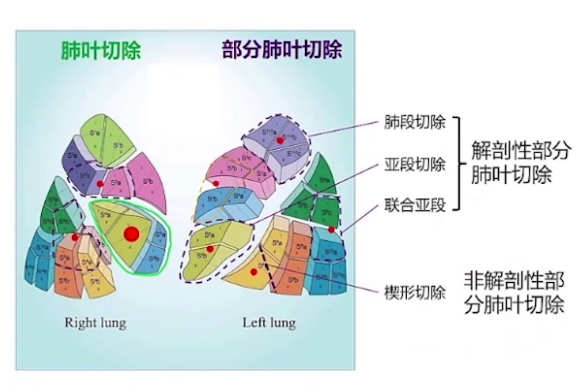
APL与经典肺段切除的区别:以下图中结节(黑点位置)为例,若行传统S1切除可能切缘不够,若行S1+S2A切除则损失肺组织过多且操作复杂。而APL首先基于安全切缘规划目标流域,其次确定受累脉管结构,然后离断相应脉管结构并显露段间界限,最后采用适形裁剪方式切除靶肺组织,既保障切缘充分,又兼顾操作简便与安全。
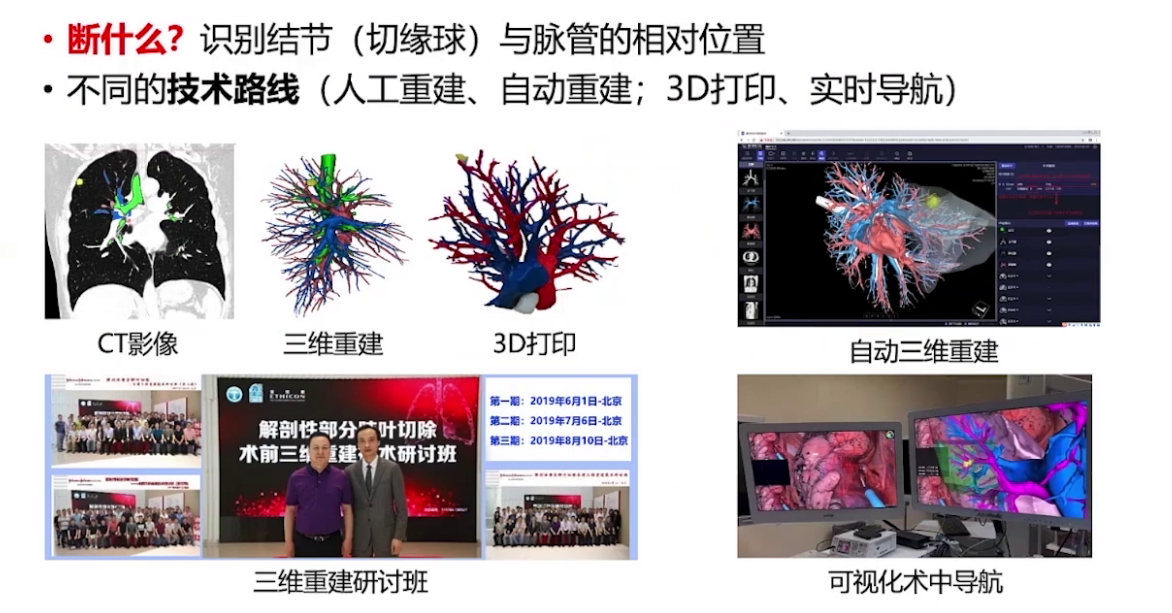
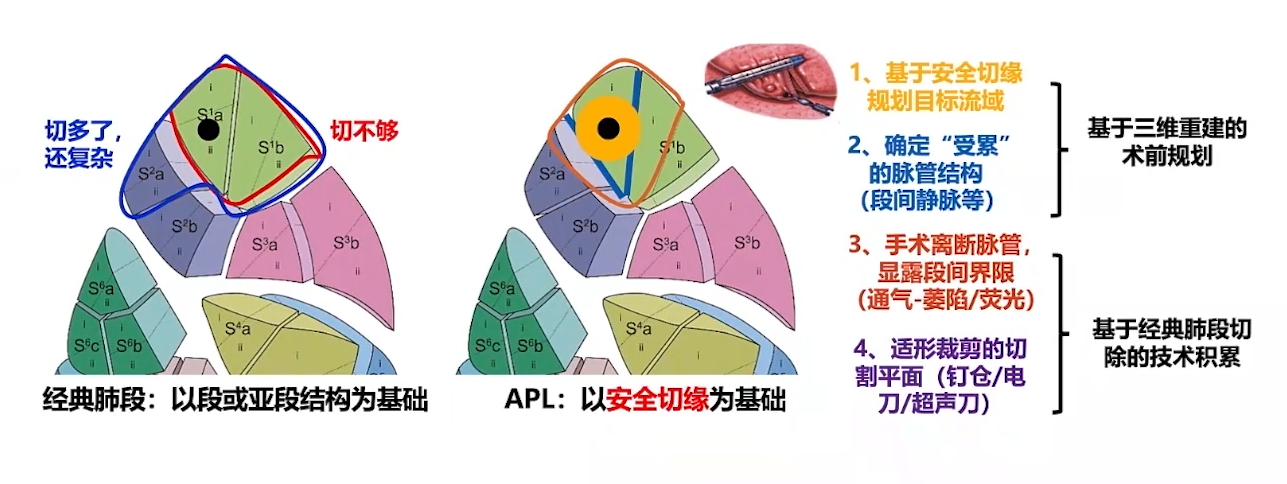 为实现APL目标,基于三维重建的术前规划与基于经典肺段切除的技术积累尤为重要。术前规划借助软件对CT影像人工三维重建结合3D打印技术,或运用精准智能软件,识别结节与脉管相对位置,明确“断什么”。自2019年起,本科通过研讨班推广三维重建技术。基于经典肺段切除的技术积累则解决“怎么断怎么切”问题,涵盖切口选择、适度解剖游离、离断技术选择、段间平面显露、切除方式选择、侧壁漏气检验、淋巴结采样等。
为实现APL目标,基于三维重建的术前规划与基于经典肺段切除的技术积累尤为重要。术前规划借助软件对CT影像人工三维重建结合3D打印技术,或运用精准智能软件,识别结节与脉管相对位置,明确“断什么”。自2019年起,本科通过研讨班推广三维重建技术。基于经典肺段切除的技术积累则解决“怎么断怎么切”问题,涵盖切口选择、适度解剖游离、离断技术选择、段间平面显露、切除方式选择、侧壁漏气检验、淋巴结采样等。
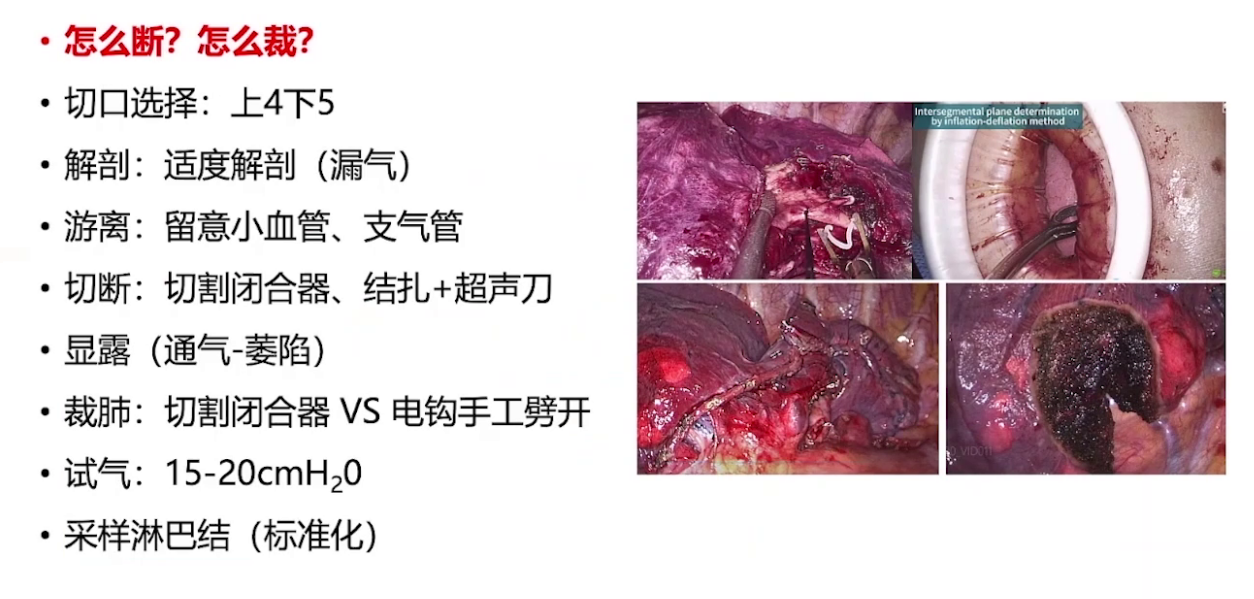
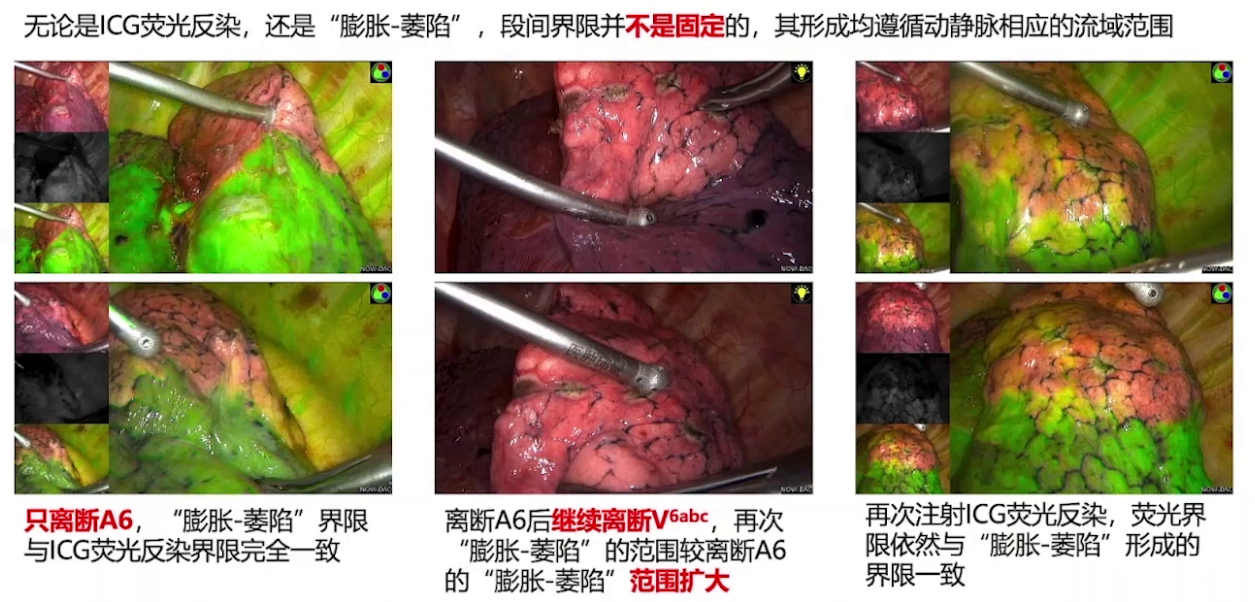
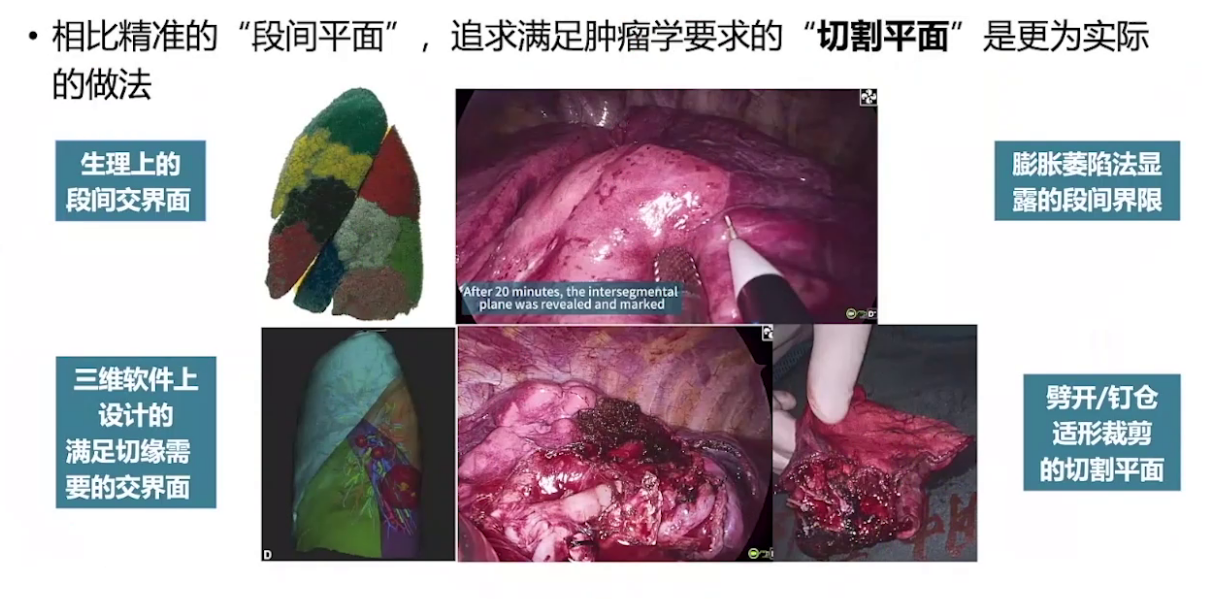
在肺段手术规划及实践中,会遇到生理上的段间交界面(不规则)、三维软件上设计满足切缘的界面(一定程度还原生理界面但不完全一致)、术中离断脉管后通气萎陷法显露的断接界限(取决于离断结构)、术中裁剪的切割平面这4种段间平面概念。因显露的断接界限不固定,追求满足肿瘤学要求的切割平面更实际。
解剖性部分肺叶切除术的特点:
(1)具有有效性,以切缘为基础设计手术方式保证肿瘤学效果;
(2)具有安全性,基本技术源于经典肺段切除术,不额外增加并发症,合理解剖理念降低手术风险,术后二级以上并发症占比约10%,持续漏气最常见;
(3)具有实用性,手术方式便于外科医生学习、实施与推广。
查看更多
专家点评
解剖性部分肺叶切除术(APL)的核心理念,是以肿瘤学原则为基础,依据肺段解剖结构进行肺组织切除。它并不强求处理肺段门部的所有结构,其核心目标是在确保切缘阴性和规范处理段门淋巴结的前提下,平衡手术的有效性、安全性及实用性,最终实现最大程度保留健康肺组织的宗旨。该术式的发展经历了两个阶段:2014-2019年,技术从单一肺段切除逐步迈向复杂的联合肺段及亚段切除,对肺段解剖的认知日趋精细化;2019-2024年,则进入了从追求解剖完全精准到强调“肿瘤学有效与手术可操作”并重的合理简化阶段,形成了涵盖术前数字化规划、术中规范化操作及术后系统评价的完整原则体系。
在适用范围上,该术式的核心适用人群为直径2cm以内、含有磨玻璃成分的周围型早期肺癌患者。其适用范围也可拓展至直径3cm以内、实性成分占比<0.5的早期肺癌病例,这恰好契合了当前临床上磨玻璃结节检出率日益升高的现状。与传统的肺叶切除术相比,APL具有显著优势:在肿瘤学效果上,多中心数据显示其5年总生存率超过96%,8年总生存率超过95%,疗效相当;在功能保留方面,它能最大限度地保留健康肺组织,显著提升患者术后生活质量;在微创特性上,微创手术占比高达99%,单孔胸腔镜技术的应用进一步减少了手术创伤,加速了术后康复。
手术的成功实施依赖于几个关键环节:首先是详尽的术前规划,必须借助三维重建技术精准定位病灶所在的肺段或亚段,并明确其与周围血管、支气管的解剖关系。其次是精细的术中操作,包括充分游离脉管结构、合理选择离断方式、运用通气萎陷法清晰显露段间平面,并注重手术细节与突发情况的应对。贯穿始终的核心要求是必须保证切缘阴性,并完成规范的淋巴结采样,从而在肿瘤根治性与手术安全性之间取得最佳平衡。