查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






2025年5月30日-6月3日,2025年美国临床肿瘤学会(ASCO)年会于美国芝加哥召开。ASCO年会是全球规模最大、最具权威的临床肿瘤学会议之一,国际顶尖专家齐聚一堂,分享最前沿的研究成果和临床实践经验,内容涵盖各种肿瘤的治疗以及相关技术和基础研究等。本届年会的主题为“推动知识转化为行动:构建更美好的未来(Driving Knowledge to Action: Building a Better Future)”。
针对大会的海量学术内容,北京大学肿瘤医院王维虎教授团队开辟【“放”眼看前沿之北京大学肿瘤医院2025年ASCO会后会系列报道】专栏,“国家队”优选放疗相关研究,带您一起掌握放疗领域最新进展,更好指导临床实践。本篇为专栏中的第一篇,由北京大学肿瘤医院王维虎、蔡勇、李永恒教授带队领学。
本期目录
01:一项评估局部晚期胆囊癌新辅助化疗对比新辅助放化疗的III期随机临床试验(POLCAGB研究)
02:肝细胞癌患者等待肝移植期间体部立体定向放疗联合或不联合其他桥接治疗的多中心比较研究
03:循环肿瘤DNA作为肛管鳞状细胞癌放化疗后的早期疗效预测指标
04:短程放疗序贯信迪利单抗联合CAPOX的全程新辅助治疗方案在局部晚期直肠癌中的应用:一项前瞻性、随机、对照研究 (SPRING-01)

研究标题:一项评估局部晚期胆囊癌新辅助化疗对比新辅助放化疗的III期随机临床试验(POLCAGB研究)
摘要号:4007 Oral
研究背景:对于初始不可R0切除的局部晚期胆囊癌(LAGBC)患者,可采用新辅助化疗(NACT)或新辅助放化疗(NACRT)使肿瘤降期并改善预后。
研究方法:本研究纳入体能状态良好的LAGBC腺癌患者,T3/T4伴肝脏侵犯(>2 cm,<5 cm);N1;梗阻性黄疸(胆道梗阻I/II型);肿瘤与十二指肠或结肠毗邻但无黏膜浸润,血管受累范围<180°。患者按1:1随机分配至NACT组(吉西他滨联合铂类化疗4周期)或NACRT组(55~57 Gy放疗同步吉西他滨,后行2周期化疗),随后评估手术可切除性。主要研究终点为总生存(OS)期,次要研究终点为无事件生存(EFS)期、R0切除率和术后并发症发生率。本次汇报期中分析结果。
研究结果:共入组124例患者(NACT组64例,NACRT组60例)。中位随访时间为62个月(范围6.9~94)。NACRT组的中位OS显著优于NACT组(21.8个月对10.1个月,P=0.006),EFS同样具有显著优势(10.6个月对4.9个月,P=0.006)。NACRT组R0切除率显著高于NACT组(51.6%对29.7%,P=0.01)。治疗结果见表1。NACRT组和NACT组的≥3级术后并发症发生率分别为9/32(28.12%)和4/22(18.18%),无显著差异(P=0.30)。
表1 治疗结果(点击查看大图)
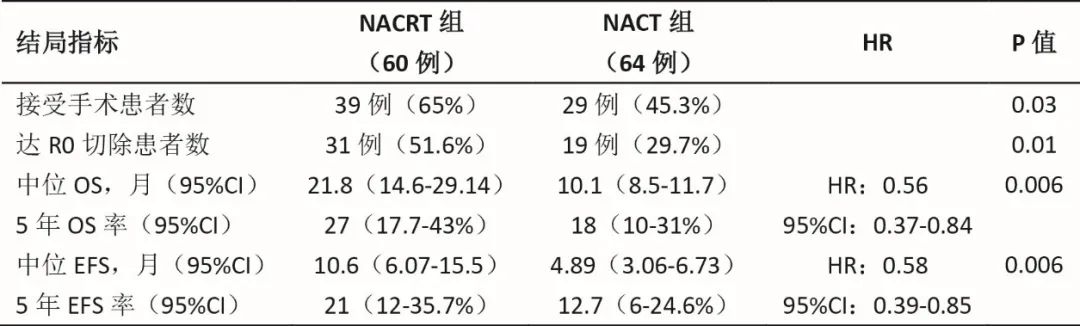
研究结论:新辅助放化疗较新辅助化疗可显著提高局部晚期胆囊癌患者的总生存期和R0切除率。


一句话点评
NACRT较NACT显著提高局LAGBC患者的总生存期和R0切除率,且未明显增加术后并发症风险,是不可切除LAGBC更优的降期治疗手段。
研究标题:肝细胞癌患者等待肝移植期间体部立体定向放疗联合或不联合其他桥接治疗的多中心比较研究
摘要号:4143 Poster
研究背景:体部立体定向放疗(SBRT)等局部治疗在肝细胞癌(HCC)患者的肝移植桥接治疗中发挥着重要的作用。本研究旨在比较单独SBRT和SBRT联合其他桥接治疗的5年随访结果。
研究方法:基于TriNetX数据库(2010-2020年),纳入符合肝移植标准且AJCC I/II期的HCC患者,分为SBRT组和联合治疗组[SBRT+经动脉化疗栓塞(TACE)和/或射频消融(RFA)]。
研究结果:匹配前,SBRT组和联合治疗组分别纳入185例和363例患者。匹配后,两组各153例患者,基线特征平衡。SBRT组和联合治疗组的5年OS率分别为61.53%和62.02%,无显著差异(HR=0.958,P=0.8417)。两组的急性肝衰竭发生率分别为22.73%和25.64%(P=0.7567),失代偿期肝硬化发生率分别为37.74%和40%(P=0.8054),治疗相关并发症发生率分别为11.61%和12.12%(P=0.9016),门静脉血栓发生率分别为12.00%和7.87%(P=0.2733),主要心血管不良事件(MACEs)发生率分别为24.75%和22.12%(P=0.6558),肾脏不良事件(急性肾损伤、慢性肾脏病、终末期肾病)发生率分别为62.75%和63.40%(P=0.9057)。
研究结论:在肝细胞癌患者肝移植桥接治疗中,单独SBRT和SBRT联合其他桥接治疗的长期生存结局相当,个别并发症的发生率存在差异。


一句话点评
对于等待肝移植的肝细胞癌患者,单用SBRT与SBRT联合其他桥接治疗(如TACE/RFA)的5年OS率无显著差异,且安全性相当,提示单用SBRT可作为有效的桥接治疗策略。
研究标题:循环肿瘤DNA作为肛管鳞状细胞癌放化疗后的早期疗效预测指标
摘要号:3518 Rapid Oral
研究背景:部分肛管鳞状细胞癌(ASCC)患者在根治性放化疗(CRT)后会出现局部区域复发(LRF)。循环肿瘤DNA(ctDNA)可用于评估疗效、预测预后,但ctDNA在ASCC中的研究相对较少。
研究方法:本研究前瞻性纳入88例接受根治性CRT的ASCC患者,纵向监测肿瘤特异性ctDNA。在三个关键时间节点检测ctDNA:治疗前(CRT开始前至开始后5天内)、治疗中(CRT开始后5天至结束前7天内)和治疗后(CRT结束前7天至结束后42天内),随后每三个月进行随访检测。分析ctDNA的动态变化与LRF、无进展生存(PFS)期之间的关系。
研究结果:治疗前79%的患者ctDNA呈阳性,治疗后92%的患者ctDNA呈阴性。中位随访时间为18个月,7例出现LRF,5例发生远处转移。治疗中ctDNA阴性患者未出现LRF,而治疗中和治疗后ctDNA阳性患者的LRF率分别为26%和61%。治疗中ctDNA阴性患者的1年PFS率为100%,而治疗中和治疗后ctDNA阳性者分别为81%和44%。7例ctDNA转阴患者在随访期间ctDNA呈阳性,并最终出现复发。所有患者ctDNA显示的分子水平的复发均早于临床或影像学证实的复发。
研究结论:在肛管鳞状细胞癌患者中,肿瘤特异性ctDNA在基线时具有较高的检出率,并在放化疗期间迅速转阴。ctDNA转阴与预后良好相关,而ctDNA检测可在临床和影像学之前提示疾病复发。


一句话点评
动态监测ctDNA能精准预测肛管鳞状细胞癌放化疗疗效与复发风险,其提示的分子水平的复发显著早于临床/影像学复发,可能是高效的预测标志物。
研究标题:短程放疗序贯信迪利单抗联合CAPOX的全程新辅助治疗方案在局部晚期直肠癌中的应用:一项前瞻性、随机、对照研究(SPRING-01)
摘要号:3519 Rapid Oral
研究背景:新辅助短程放疗(SCRT)联合化疗的全程新辅助治疗(TNT)方案可提高局部晚期直肠癌(LARC)的病理完全缓解(pCR)率,而放疗联合免疫的潜在协同效应可能使LARC患者进一步获益。本研究旨在对比在LARC患者中,短程放疗序贯6周期CAPOX方案化疗联合或不联合免疫治疗的疗效和安全性。
研究方法:该项随机对照研究中,T3-4、N+、EMVI+、MRF+或侧方淋巴结阳性的直肠腺癌患者被随机分配接受SCRT序贯6周期CAPOX方案化疗、联合或不联合信迪利单抗的TNT方案。并在完成TNT后2~3周内接受直肠全系膜切除术(TME)。主要研究终点是pCR率。
研究结果:放化免组和放化组各49例患者,pCR率分别为59.2%和32.7%,分别有30(61.2%)例、16(32.7%)例患者达到完全缓解(CR,包括病理完全缓解pCR和临床完全缓解cCR)。放化免组和放化组分别有45例、44例患者接受手术,TRG分级(AJCC第8版)为0级的患者分别为29(64.4%)例、16(36.4%)例,TRG分级1级的患者分别为7(15.6%)例、7(15.9%)例,TRG分级2级的患者分别为5(11.1%)例、13(29.5%)例,TRG分级3级的患者分别为4(8.9%)例、8(18.2%)例。安全性方面,放化免组和放化组分别有29(59%)例、27(55%)例患者发生1~2级治疗相关不良反应(TRAEs),15(31%)例、16(33%)例患者发生3级TRAEs。放化免组有1(2%)例患者发生4级TRAE,放化组有1(2%)例患者发生5级TRAE。
研究结论:对于局部晚期直肠癌患者,短程放疗联合CAPOX+信迪利单抗的新辅助治疗方案显著提高了病理完全缓解率,且安全性可控,可作为T3-4、N+、EMVI+、MRF+或侧方淋巴结阳性的直肠癌患者全程新辅助治疗的优选方案。


一句话点评
本研究结果提示局部晚期直肠癌短程放疗联合化疗及免疫治疗的全程新辅助治疗模式带来了较为理想的完全缓解率,高于既往多项研究报道的结果,为直肠癌患者器官保留带来了更多可能。
领衔专家丨北京大学肿瘤医院 王维虎 蔡勇 李永恒
校译丨北京大学肿瘤医院 杜荣旭 郑宣
翻译丨北京大学肿瘤医院 冯佳琳 李思萱
通讯员丨北京大学肿瘤医院 滕悦



博士、博士后导师
北京大学肿瘤医院 放疗科主任
主编《中国原发性肝细胞癌放射治疗指南》
主编《消化、头颈、胸部肿瘤放疗规范和靶区定义》系列丛书
中国医师协会放射肿瘤治疗医师分会 常委
中国医师协会放射肿瘤治疗医师分会肝癌放疗学组 组长
中华医学会放射肿瘤治疗学分会 全国委员
中华医学会放射肿瘤治疗学分会肝癌放疗学组 副组长
北京医学会放射肿瘤治疗学分会 候任主任委员
北京医师协会放射治疗专科医师(技师)分会 副会长
北京癌症防治学会消化道肿瘤放疗专业委员会 主任委员
获中华医学科技二等奖和北京市科学技术奖三等奖
在《癌细胞》(Cancer Cell)、《美国医学会·外科学》(JAMA Surgery)、《肝病学》(Hepatology)等发表论文100余篇

北京大学肿瘤医院放射治疗科多年来一直致力于肿瘤的规范化诊治,个体化放疗及多学科综合治疗等。科室以“团结创新,至仁至精”为科训,通过具体项目带领全科进步,借助规范提升临床和科研水平,并努力实现肿瘤领域引领和示范作用。团队年收治新患者约5000例,正在进行的临床试验50余项,在研各类课题24项,在《美国医学会杂志·外科学》(JAMA Surgery)、《柳叶刀·肿瘤学》(Lancet Oncol)、《肝病学》(Hepatology)、《国际放射肿瘤学·生物学·物理学杂志》(IJROBP)、《放射治疗学及肿瘤学》(Radiother Oncol)等期刊上发表科学论文多篇,并主编了《恶性肿瘤放疗规范和靶区定义》系列丛书。
查看更多